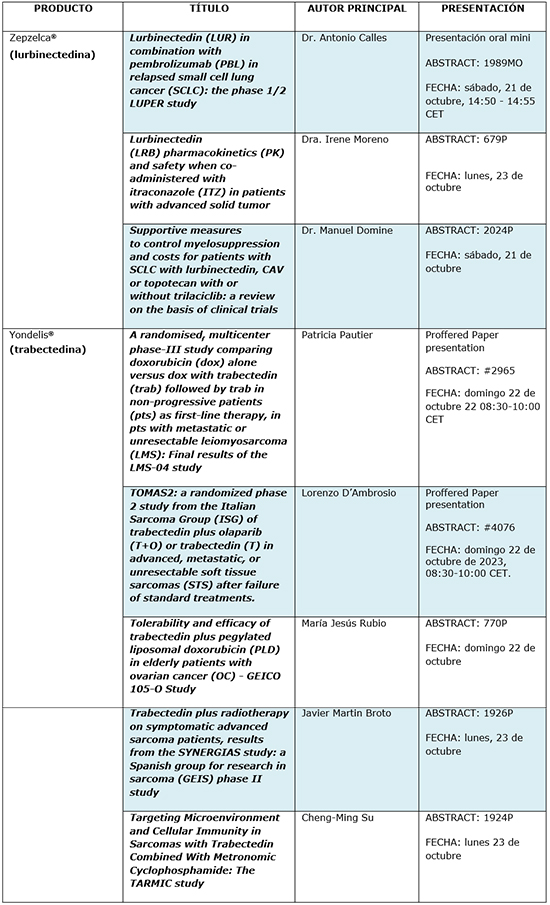
PharmaMar (MSE:PHM) ha anunciado hoy que presentará nuevos datos sobre lurbinectedina en cáncer de pulmón de célula pequeña (CPCP) en el congreso de la Sociedad Europea de Oncología Médica (ESMO), que se celebra en Madrid del 20 al 24 de octubre. Entre los estudios más destacados habrá una presentación oral del Dr. Antonio Calles, donde, por primera vez, se presentan datos finales del ensayo LUPPER de lurbinectedina en combinación con inmunoterapia en segunda línea de CPCP. El abstract llamado “Lurbinectedin (LUR) in combination with pembrolizumab (PBL) in relapsed small cell lung cancer (SCLC): the phase 1/2 LUPER study” concluye que la combinación de lurbinectedina y pembrolizumab es un tratamiento de segunda línea eficaz para el CPCP en pacientes que no recibieron inmunoterapia previa, logrando en algunos casos respuestas profundas y duraderas, con un perfil de seguridad manejable y sin nuevas señales de toxicidad emergentes al combinar los dos fármacos. El Dr. Antonio Calles, Médico Especialista en Oncología Médica del Hospital General Universitario Gregorio Marañón, Madrid, España, que ha liderado el estudio comenta que “la combinación representa una oportunidad para aquellos pacientes con cáncer microcítico de pulmón metastásico que no pudieron ser tratados con inmunoterapia en primera línea. El tratamiento logró una tasa de respuestas confirmada del 46,4%, incluidas respuestas profundas y duraderas que sobrepasaron el año en algunos pacientes. La mediana de la supervivencia libre de progresión (SLP) fue significativamente más larga para los pacientes sensibles al platino en comparación con los pacientes resistentes al platino, con una SLP de 10 versus 3 meses, respectivamente. En la actualidad, el único tratamiento aprobado para esta indicación en las últimas 2 décadas tiene una tasa de respuestas de sólo el 20% y una SLP de 4 meses, además de una toxicidad muy significativa. Por otro lado, no se observaron efectos secundarios inesperados y se pudo combinar de forma segura y a dosis completas ambos fármacos”. El Dr. Ali Zeaiter, Vicepresidente y Director de Desarrollo Clínico de PharmaMar comenta "nos complace presentar nuevos datos sobre la combinación de lurbinectedina con inmunoterapia. Creemos que estos datos, con las mejoras sugeridas en los resultados de los pacientes, confirman una vez más que lurbinectedina es una opción de tratamiento importante para el CPCP recidivante y apoyan la investigación adicional de la combinación de lurbinectedina con inmunoterapia". Además, de la presentación anterior, el abstract titulado “A randomised, multicenter phase-III study comparing doxorubicin (dox) alone versus dox with trabectedin (trab) followed by trab in non-progressive patients (pts) as first-line therapy, in pts with metastatic or unresectable leiomyosarcoma (LMS): Final results of the LMS-04 study” presentará los datos finales de supervivencia global (OS overall survival) de la combinación de doxorrubicina y trabectedina. Esta combinación obtuvo un beneficio clínicamente significativo frente a doxorrubicina, 33,1 meses frente a 23,8 meses. Estos datos confirman que esta es la primera combinación de fármacos que es capaz de demostrar beneficio tanto en SLP como en OS en un ensayo fase III en primera línea de tratamiento en leiomiosarcomas metastásicos. Estos datos apoyan aún más la justificación de estudiar también lurbinectedina en sarcoma. La Dra. Patricia Pautier, del Institut Gustave Roussy en Villejuif, París, Francia, comenta “los resultados finales fueron positivos, con una mediana de supervivencia libre de progresión (SLP) mejorada estadísticamente de 6,2 meses con doxorrubicina sola, a 12,2 meses con la combinación” Abstracts de PharmaMar en ESMO 2023
Aviso El presente comunicado no constituye una oferta de venta o la solicitud de una oferta de compra de valores, y no constituirá una oferta, solicitud o venta en cualquier jurisdicción en la que dicha oferta, solicitud o venta sea ilegal antes del registro o verificación bajo las leyes de valores de dicha jurisdicción. Sobre Yondelis® Yondelis® (trabectedina) es un compuesto antitumoral producido sintéticamente y aislado originalmente de la Ecteinascidia turbinata, un tipo de ascidia. Yondelis® ejerce sus efectos anticancerígenos principalmente mediante la inhibición de la transcripción activa, un tipo de expresión génica del que dependen especialmente las células cancerígenas que proliferan. Sobre Zepzelca® Zepzelca® (lurbinectedina), también conocido como PM1183, es un análogo del compuesto de origen marino ET-736, aislado de la ascidia Ecteinacidia turbinata, donde un átomo de hidrógeno ha sido reemplazado por un grupo de metoxi. Es un inhibidor selectivo de los programas de transcripción oncogénica de los que muchos tumores son particularmente dependientes. Junto con su efecto sobre las células cancerosas, lurbinectedina inhibe la transcripción oncogénica en macrófagos asociados al tumor, disminuyendo la producción de citoquinas que son esenciales para el crecimiento del tumor. La adicción a la transcripción es un objetivo reconocido en esas enfermedades, muchas de las cuales carecen de otros objetivos procesables. Fuente: PharmaMar |