Alertas
-

Fulvestrant DR. Reddys 250 mg solución inyectable en jeringa precargada EFG, 2 jeringas precargadas de 5 ml + 2 agujas (NR: 82518, CN: 719459)
13/03/2024 | ALERTAS
-

Pleinvue polvo para solución oral, 3 (1x3) sobres (NR: be518640, CN: 729190)
21/02/2024 | ALERTAS
-

Imunocare 50 mg/g crema 24 sobres unidosis de 250 mg (NR: 78406, CN: 701283)
13/02/2024 | ALERTAS
-

Metformina Vir 850 mg comprimidos recubiertos con película EFG , 50 comprimidos (NR: 72708, CN: 681987)
13/02/2024 | ALERTAS
-

Sugammadex Orion 100 mg/ml solución inyectable EFG, 10 viales de 5 ml (NR: 88751, CN: 762459)
23/01/2024 | ALERTAS
-

Sugammadex Sala 100 mg/ml solución inyectable EFG, 10 viales de 5 ml (NR: 88700, CN: 607631)
23/01/2024 | ALERTAS
-
Ver todas las alertas
Problemas de suministro
-

PACLITAXEL ACCORD 6 mg/ml Concent. para sol. para perfus. env. con 1 vial de 16,7 ml
-

TROMALYT 300 mg Cáps. dura de liberación prolongada env. con 500
-

GLIMEPIRIDA VIATRIS 4 mg Comp. env. con 120
-

SANDOSTATIN 100 mcg/ml Sol. iny. y para perfus. env. con 5 ampollas de 1 ml
-

SANDOSTATIN 50 mcg/ml Sol. iny. y para perfus. env. con 5 ampollas de 1 ml
-

LEVOFLOXACINO SANDOZ 500 mg Comp. recub. con película env. con 7
-
Ver todos los Problemas de Suministro
Actualización de monografía de principios activos
-
AVAPRITINIB (18/04/2024) MONOGRAFÍA DE NUEVO PRINCIPIO ACTIVO EN ESPAÑA
-
RIPRETINIB (17/04/2024) MONOGRAFÍA DE NUEVO PRINCIPIO ACTIVO COMERCIALIZADO EN ESPAÑA
-
RELUGOLIX (17/04/2024) MONOGRAFÍA DE NUEVO PRINCIPIO ACTIVO COMERCIALIZADO EN ESPAÑA.
-
ESPESOLIMAB (17/04/2024) MONOGRAFÍA DE NUEVO PRINCIPIO ACTIVO COMERCIALIZADO EN ESPAÑA
-
TRAMADOL Y CELECOXIB (17/04/2024) MONOGRAFÍA DE NUEVO PRINCIPIO ACTIVO COMERCIALIZADO EN ESPAÑA
-
LATANOPROST Y NETARSUDIL (17/04/2024) MONOGRAFÍA DE NUEVO PRINCIPIO ACTIVO COMERCIALIZADO EN ESPAÑA
Noticias
-

Un estudio analizará el beneficio del consumo de vino moderado en mayores de 50 años
07/05/2024 | PUBLICACIONES
-

La reunión de zona de la SEFH en Baleares apuesta por el valor del Farmacéutico Hospitalario en las pruebas de genómica
07/05/2024 | JORNADAS
-

Angelini Pharma y ESADE premian la mejor propuesta para combatir el nihilismo terapéutico en epilepsia
06/05/2024 | PATOLOGÍAS
-
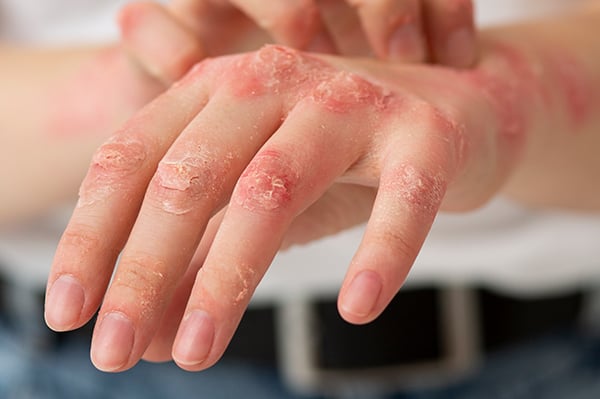
La calidad de vida de las personas con psoriasis pustulosa generalizada protagoniza el último vídeo de la campaña `Enfermedades raras de la piel´ de Boehringer Ingelheim
06/05/2024 | PATOLOGÍAS
-
Quirónsalud Infanta Luisa señala la osteotomía periacetabular como alternativa a la prótesis en jóvenes con displasia de cadera
06/05/2024 | TECNOLOGÍA
-

Recomendaciones para una fotoprotección eficaz ante los primeros rayos de sol
06/05/2024 | PUBLICACIONES
-
Ver todas las noticias

