Propiedades farmacocinéticas: La farmacocinética de sunitinib y malato de sunitinib ha sido evaluada en 135 voluntarios sanos y en 266 pacientes con tumores sólidos.
Absorción: Las concentraciones plasmáticas máximas (Cmáx.) se observaron generalmente entre 6-12 horas (Tmáx.) después de la administración oral. Los alimentos no afectaron la biodisponibilidad de sunitinib.
Distribución: La unión in vitro de sunitinib y de su metabolito primario activo a las proteínas plasmáticas humanas fue de 95 y 90%, respectivamente, sin aparente dependencia con la concentración en el rango de 100-4000 ng/ml. El volumen de distribución aparente (Vd/F) de sunitinib fue grande —2230 L—, indicando su distribución hacia los tejidos. En el rango de dosis de 25-100 mg, el área bajo la curva de concentración plasmática-tiempo (ABC) y la Cmáx. aumentaron proporcionalmente con la dosis.
Metabolismo: Los valores de Ki calculados para todas las isoformas CYP evaluadas in vitro (CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4/5 y CYP4A9/11) indicaron que es improbable que el sunitinib y su metabolito activo principal tengan interacciones clínicamente relevantes con medicamentos que puedan ser metabolizados por estas enzimas.
Estudios in vitro indicaron que sunitinib no induce ni inhibe enzimas CYP principales, incluyendo CYP3A4 (véase Interacciones medicamentosas y de otro género).
El sunitinib es metabolizado principalmente por la enzima del citocromo P-450, CYP3A4, para producir su metabolito activo principal, que posteriormente es metabolizado por CYP3A4. El metabolito activo principal abarca de 23 a 37% de la exposición total.
Eliminación: La excreción ocurre principalmente vía heces (61%) con eliminación renal del medicamento y sus metabolitos correspondientes al 16% de la dosis administrada. El sunitinib y su metabolito activo principal fueron los principales compuestos relacionados con el medicamento identificados en plasma, orina y heces, representando 91.5, 86.4 y 73.8% de la radiactividad en muestras combinadas, respectivamente. Se identificaron metabolitos menores en orina y heces, pero generalmente no se detectaron en el plasma. La depuración oral total (CL/F) varió entre 34-62 L/hr con una variabilidad interpaciente de 40%. Después de la administración de una dosis oral individual en voluntarios sanos, el tiempo de vida media terminal de sunitinib y su metabolito activo primario desetilo fueron de aproximadamente 40-60 horas y 80-110 horas, respectivamente.
Farmacocinética en grupos especiales de pacientes:
Insuficiencia hepática: Sunitinib y su metabolito activo son principalmente metabolizados mediante el hígado. Las exposiciones sistémicas tras una dosis única de sunitinib fueron similares en sujetos con deterioro hepático leve (Child-Pugh Clase A) o moderado (Child-Pugh Clase B) en comparación con sujetos con funcionamiento hepático normal. El sunitinib no ha sido estudiado en sujetos con deterioro hepático severo (Child-Pugh Clase C).
Insuficiencia renal: Los análisis farmacocinéticos de la población demostraron que la farmacocinética de sunitinib se mantuvo inalterada en los pacientes con depuraciones de creatinina calculadas en el rango de 42-347 ml/min. Las exposiciones sistémicas tras una toma única de sunitinib fueron similares en sujetos con insuficiencia renal severa (Dep. creat.r < 30 ml/min) comparado con sujetos con función renal normal (Dep. creat. > 80 ml/min). Aunque sunitinib y su metabolito primario no fueron eliminados a través de la hemodiálisis en sujetos con enfermedad renal en etapa terminal (ERET), la exposición sistémica total resultó 47% más baja para sunitinib y 31% para su metabolito primario en comparación con los sujetos con función renal normal.
Electrofisiología cardiaca: Se investigó la prolongación del intervalo QT en un estudio en fase 1 con 24 pacientes evaluables, con edad de 20-87 años con malignidades avanzadas. A concentraciones plasmáticas terapéuticas, el cambio promedio de QTcF (corrección de Frederica) máximo desde la línea basal fue 9.6 mseg (CI del 95%, 15.1 mseg). A aproximadamente el doble de las concentraciones terapéuticas, el cambio promedio de QTcF máximo desde la línea basal fue 15.4 mseg (CI del 90%, 22.4 mseg). La moxifloxacina (400 mg) utilizada como un control positivo mostró un cambio QTcF promedio máximo de 5.6 mseg desde la línea basal. Ningún sujeto experimentó un efecto sobre el intervalo QTc mayor al grado 2 (CTCAE v.3.0). Ningún paciente presentó arritmia cardiaca (véase Precauciones generales).
Farmacocinética plasmática: Después de la administración de una sola dosis oral a voluntarios sanos, las vidas medias de eliminación de sunitinib y su metabolito activo principal fueron aproximadamente 40-60 horas y 80-110 horas, respectivamente. Con la administración diaria repetida, el sunitinib se acumuló de 3 a 4 veces, mientras que el metabolito activo principal se acumuló de 7 a 10 veces. Las concentraciones en estado estable de sunitinib y su metabolito activo principal se alcanzan en el lapso de 10 a 14 días. En el día 14, las concentraciones plasmáticas combinadas de sunitinib y su metabolito activo son de 62.9-101 ng/ml, que son las concentraciones meta predichas con base en los datos preclínicos, capaces de inhibir in vitro la fosforilación del receptor y que resultan en la reducción del crecimiento/estancamiento tumoral in vivo. No se observaron cambios significativos en la farmacocinética de sunitinib o del metabolito activo principal con la administración diaria repetida ni con la repetición de los ciclos en los regímenes de dosificación evaluados.
Las farmacocinéticas fueron similares en todas las poblaciones de tumores sólidos evaluados y en los voluntarios sanos.
Farmacocinética de la población: Los análisis farmacocinéticos de la población de los datos demográficos indicaron que no hubo efectos clínicamente relevantes de la edad, peso corporal, depuración de creatinina, género, raza o calificación ECOG (por sus siglas en inglés) sobre la farmacocinética de sunitinib o del metabolito activo principal.
Peso, estado de desempeño: Los análisis farmacocinéticos de la población de los datos demográficos indican que no hay ajustes de la dosis inicial por peso o el desempeño del Grupo de Oncología de Cooperativa Oriental (ECOG, por sus siglas en inglés).
Género: Los datos disponibles indican que las mujeres pueden tener una depuración aparente (CL/F) de sunitinib menor que los hombres en aproximadamente 30%: esta diferencia, sin embargo, no necesita ajustes en dosis inicial.
Propiedades farmacodinámicas: Sunitinib inhibe múltiples receptores de tirosina cinasa (RTK) que están implicados en el crecimiento tumoral, angiogénesis patológica, y progresión metastásica del cáncer. Sunitinib fue identificado como un inhibidor de receptores del factor de crecimiento derivado de plaquetas (PDGFR? y PDGFRß), receptores del factor de crecimiento del endotelio vascular (VEGFR1, VEGFR2 y VEGFR3), receptor del factor de células madre (KIT), tirosina cinasa-3 (FLT3) similar a Fms, receptor del factor estimulador de colonias Tipo 1 (CSF-1R), y receptor del factor neurotrófico derivado de la línea de células gliales (RET). La inhibición que ejerce sunitinib sobre la actividad de estos RTK se ha demostrado en ensayos bioquímicos y celulares, y la inhibición de la función se ha demostrado en ensayos de proliferación celular. El metabolito primario presenta una potencia similar comparada con la de sunitinib en ensayos bioquímicos y celulares.
El sunitinib inhibió la fosforilación de múltiples RTK (PDGFRß, VEGFR2, KIT) en injertos tumorales con expresión de blancos RTK in vivo y demostró capacidad de inhibición del crecimiento tumoral o regresión tumoral y/o inhibió las metástasis en algunos modelos experimentales de cáncer. El sunitinib demostró capacidad para inhibir in vitro el crecimiento de células tumorales expresando blancos RTK no-regulados (PDGFR, RET o KIT) para inhibir in vivo la angiogénesis tumoral, dependiendo del PDGFRß y del VEGFR2.
Estudios clínicos: La seguridad y la eficacia clínica de sunitinib se ha estudiado en pacientes con tumores del estroma gastrointestinal (GIST) resistentes al imatinib (es decir, en quienes experimentaron progresión de la enfermedad durante o después del tratamiento con imatinib) o en pacientes intolerantes al imatinib (es decir, en quienes experimentaron una toxicidad significativa durante el tratamiento con imatinib, que impidió seguir el tratamiento), así como en pacientes con carcinoma de células renales metastásico (CCRm).
La eficacia se estableció con base en el tiempo transcurrido hasta la progresión del tumor (TTP, por sus siglas en inglés) y en un aumento de la supervivencia para el CCRm.
La eficacia se estableció con base en la supervivencia libre de progresión (SLP) y en los índices de respuesta objetiva (IRO) para CCRm nunca tratado y refractario a las citocinas, respectivamente.
Tumores del estroma gastrointestinal (GIST): Se realizó un estudio inicial, abierto, con escalamiento de dosis, en pacientes con GIST, después del fracaso del imatinib (mediana de la dosis diaria máxima 800 mg) debido a resistencia o intolerancia. Se reclutaron 97 pacientes para diferentes dosis y duración de los regímenes de tratamiento; 55 pacientes recibieron 50 mg con el régimen de dosificación recomendado de 4 semanas sí/2 semanas no (“Régimen 4/2”). En este estudio, la mediana de TTP y SLP fue de 34.0 semanas (CI del 95% = 22.0-46.0 semanas).
Se realizó un estudio en fase 3 con sunitinib, con distribución aleatoria, doble ciego, controlado con placebo, en pacientes con GIST que no toleraron, o experimentaron progresión de la enfermedad, durante o después del tratamiento con imatinib (mediana de la dosis diaria máxima 800 mg). En este estudio, 312 pacientes fueron distribuidos aleatoriamente (2:1) para recibir 50 mg de sunitinib o placebo por vía oral una vez al día, aplicando el Régimen 4/2, hasta la progresión de la enfermedad o retiro del estudio por algún otro motivo (207 pacientes recibieron sunitinib y 105 pacientes recibieron placebo). El criterio de valoración de eficacia primaria del estudio fue el TTP (valorado mediante la revisión independiente), definido como el tiempo transcurrido desde la distribución aleatoria, hasta la primera documentación de progresión objetiva del tumor. Los objetivos secundarios incluyeron SLP, IRO y supervivencia global (SG).
En el momento de efectuarse el análisis preliminar previamente especificado, la mediana de TTP en sunitinib fue de 28.9 semanas (95% CI = 21.3-34.1 semanas), evaluado por el Investigador y 27.3 semanas (95% CI = 16.0-32.1 semanas) evaluado por el comité de monitoreo y seguridad de datos, un incremento estadísticamente significativo que el TTP de 5.1 semanas (95% CI = 4.4-10.1 semanas) que el evaluado por el Investigador y 6.4 semanas (95% CI = 4.4-10.0 semanas) que el evaluado por el comité de monitoreo y seguridad de datos. La diferencia en supervivencia general fue estadísticamente a favor del sunitinib [proporción de riesgo: 0.491 (95% CI 0.290-0.831)]; el riesgo de muerte fue dos veces mayor en pacientes en el grupo de placebo comparado con el grupo de sunitinib. Información adicional de eficacia se presenta a continuación en la tabla 1.
Después del análisis preliminar positivo de eficacia y seguridad, a recomendación independiente del comité de monitoreo y seguridad de datos (DSMB, por sus cifras en inglés), se suspendió el cegamiento del estudio y se ofreció a los pacientes en el grupo de placebo, un tratamiento de sunitinib de etiqueta abierta.
Un total de 255 pacientes recibieron sunitinib en la fase de tratamiento no cegada del estudio, Incluyendo 99 pacientes quienes se trataron inicialmente con placebo. En este análisis final, el grupo de placebo incluyó aquellos pacientes aleatorizados al placebo quienes posteriormente recibieron el tratamiento de sunitinib.
Los análisis finales de criterios de valoración primarios y secundarios del estudio reafirmaron los resultados obtenidos en el tiempo del análisis preliminar, como se muestra en la tabla 1 a continuación:
Tabla 1. Resumen de criterios de valoración de eficacia (población ITT)
| Criterio de valoración | Tratamiento doble ciego |
| Mediana (95% CI) | Proporción de peligro | Tratamiento b del grupo cruzado de placebo |
| Sunitinib | Placebo | (95% CI) | p |
| Primario TTP (semanas) |
| Preliminar | 27.3 (16.0 a 32.1) | 6.4 (4.4 a 10.0) | 0.329 (0.233 a 0.466) | < 0.001 | - |
| Final | 26.6 (16.0 a 32.1) | 6.4 (4.4 a 10.0) | 0.339 (0.244 a 0.472) | < 0.001 | 10.4 (4.3 a 22.0) |
| Secundario |
| Preliminar |
| SLP (semanas) c | 24.1 (11.1 a 28.3) | 6.0 (4.4 a 9.9) | 0.333 (0.238 a 0.467) | < 0.001 | - |
| IRO (%) d | 6.8 (3.7 a 11.1) | (0)- | NA | 0.006 | - |
| SG (semanas) e | - | - | 0.491 (0.290 a 0.831) | 0.007 | - |
| Final |
| SLP (semanas) | 22.9 (10.9 a 28.0) | 6.0 (4.4 a 9.7) | 0.347 (0.253 a 0.475) | < 0.001 | - |
| IRO (%) d | 6.6 (3.8 a 10.5) | (0)- | NA | 0.004 | 10.1 (5.0 a 17.8) |
| RG (semanas) | 72.7 (61.3 a 83.0) | 64.9 (45.7 a 96.0) | 0.876 (0.679 a 1.129) | 0.306 | - |
a Los resultados del tratamiento doble ciego pertenecen a la población ITT y se utiliza la medida de radiólogo central, como sea apropiado.
b Los resultados de eficacia para los 99 sujetos quienes pasaron del tratamiento con placebo a sunitinib después de la interrupción del cegamiento. La línea basal se reajustó al momento del cambio y los análisis de eficacia se basaron en la evaluación de los investigadores.
c Los números SLP preliminares se han actualizado con base en el recálculo de los datos originales.
d Los resultados de IRO se presentan como el porcentaje de sujetos con respuesta confirmada con el IC 95%.
e No se alcanzó la mediana porque los datos no eran maduros todavía.
De aquellos pacientes aleatorizados al grupo sunitinib, 62.7% sobrevivieron más de un año. 35.5% sobrevivieron más de 2 años y 22.3% sobrevivieron más de 3 años.
En general, el estudio demostró una mejora estadística y clínicamente significativa en TTP, el criterio de valoración primario, para sunitinib más el mejor cuidado de soporte comparado con el mejor cuidado de soporte más placebo.
Carcinoma de células renales:
CCRm nunca tratado: Se realizó un estudio aleatorizado en fase 3 para comparar el sunitinib como agente único con el IFN-α en pacientes con CCRm nunca tratado. El objetivo primario fue comparar PFS en pacientes que recibieron sunitinib versus pacientes que recibieron IFN-α. Los objetivos secundarios incluyeron seguridad de TTP, IRO, SG y los resultados reportados por los pacientes (RRP). Setecientos cincuenta (750) pacientes fueron distribuidos aleatoriamente (1:1) para recibir 50 mg de sunitinib una vez al día con el Régimen 4/2 o para recibir IFN-α administrado subcutáneamente a 9 MIU tres veces a la semana.
Los pacientes son tratados hasta la progresión de la enfermedad o el retiro del estudio por otro motivo.
La población ITT para este análisis interino incluyó 750 pacientes, 375 distribuidos aleatoriamente a sunitinib y 375 a IFN-α. El estado de desempeño de ECOG, la raza, género y edad basales fueron comparables y balanceados entre los grupos de sunitinib e IFN-α. En la tabla 2 se muestran las características demográficas y de los pacientes. El sitio más común que presentó metástasis en la selección fue el pulmón (78 vs 80%, respectivamente), seguido por los ganglios linfáticos (58 vs 53%, respectivamente), y los huesos (30% en cada grupo); la mayoría de los pacientes tuvo sitios metastásicos múltiples (2 o más) en la línea basal (80 vs 77%, respectivamente).
Tabla 2. Línea basal de demografía en el estudio de primer tratamiento para CCRm
| Primer tratamiento para CCR |
Sunitinib
(n = 375) | IFN-α
(n = 375) |
| Género [n(%)] |
| Masculino | 267 (71) | 269 (72) |
| Femenino | 108 (29) | 106 (28) |
| Raza autoidentificada [n(%)] |
| Blanco | 354 (94) | 340 (91) |
| Asiático | 7 (2) | 12 (3) |
| Negro | 4 (1) | 9 (2) |
| Sin reportar | 10 (3) | 14 (4) |
| Grupo de edad [n (%)] |
| < 65 años | 223 (59) | 252 (67) |
| ≥ 65 años | 152 (41) | 123 (33) |
| Apropiado estado general [n (%)] |
| 0 | 231 (62) | 229 (61) |
| 1 | 144 (38) | 142 (38) |
| 2 | 0 (0) | 4 (1)a |
| Tratamiento anterior [n (%)] |
| Nefrectomía | 340 (91) | 335 (89) |
| Radioterapia | 53 (14) | 54 (14) |
a Los pacientes tuvieron apropiado estado general ECOG GOCO de 1 durante el escrutinio, que cambió a 2 en la línea basal.
La duración media del tratamiento fue de 11.1 meses (rango: 0.4-46.1) para el tratamiento con sunitinib y 4.1 meses (rango: 0.1-45.6) para tratamiento con IFN-α. Las interrupciones de dosis ocurrieron en 202 pacientes (54%) en sunitinib y 141 pacientes (39%) en IFN-α. Las reducciones de dosis ocurrieron en 194 pacientes (52%) en sunitinib y 98 pacientes (27%) en IFN-α. La razón de descontinuación debida a reacciones adversas fueron 20% para sunitinib y 23% para IFN-α. Los pacientes fueron tratados hasta la progresión de la enfermedad o retiro del estudio. El criterio de valoración de eficacia primaria fue la supervivencia libre de progresión (SLP). Un análisis preliminar planeado mostró una ventaja estadísticamente significativa para el sunitinib sobre el IFN-α en el criterio de valoración primario de SLP, con SLP para sunitinib más del doble que para IFN-α (47.3 y 22.0 semanas, respectivamente). El criterio de valoración secundario de IRO fue más de cuatro veces mayor para sunitinib que para IFN-α (27.5% y 5.3%, respectivamente). Los datos no estaban suficientemente maduros para determinar el beneficio de supervivencia general; en el tiempo de este análisis preliminar, 374 de 750 pacientes reclutados (50%) continuaron en el estudio, 248/375 (66%) en el grupo de sunitinib y 126/375 (34%) en el grupo de IFN-α.
En el momento del análisis final hubo una ventaja estadística significativa para el sunitinib sobre el IFN-α en el criterio de valoración de SLP (véase tabla 3 y figura 1). En los factores preespecíficos de estratificación de DHL (> 1.5 LSN contra ≤ 1.5 LSN), el estado funcional ECOG (0 contra 1), y antes de la nefrectomía (sí contra no), la proporción de peligro favoreció a sunitinib sobre IFN. La evaluación por radiología central se descontinuó una vez que se alcanzó el criterio de valoración primario. El IRO determinado por la evaluación de los investigadores fue de 46% (IC de 95%: 41,51) para el grupo de sunitinib y 12% (IC de 95%: 9,16) para el grupo IFN-α (p<0.001) (véase tabla 3).
Los resultados fueron similares en los análisis de soporte y fueron robustos al controlar la demografía (edad, género, raza y estado funcional) y los factores de riesgo conocidos. Para 262 de 750 pacientes (35%) sin factores de riesgo MSKCC, la mediana SLP fue 64.1 semanas en el grupo sunitinib y 34.1 semanas en el grupo IFN-α (HR 0.447, 95% CI [0.313-0.640]); para 424 pacientes (56%) con 1 ó 2 factores de riesgo, la mediana PFS fue 46.6 semanas en el grupo sunitinib y 16.1 semanas en el grupo IFN-α (HR 0.547, IC de 95% [0.423-0.707]); y para 47 pacientes (6%) con ≥ 3 factores de riesgo, la mediana de SLP fue de 12.1 semanas en el grupo de sunitinib y 5.7 semanas en el grupo IFN-α (HR 0.679, IC 95% [0.330-1.398]).
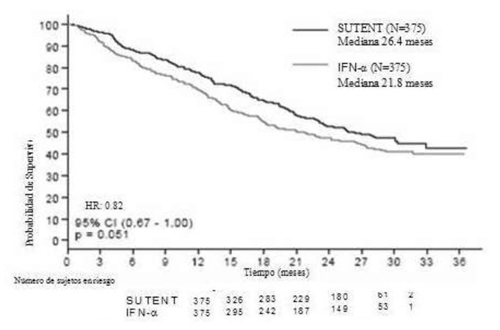
Como se muestra en la Figura 2, el tratamiento de sunitinib fue asociado con supervivencia mayor en comparación con IFN-α. La mediana de SG fue 114.6 semanas para el grupo de sunitinib (IC de 95%: 100.1-142.9) y 94.9 semanas para el grupo IFN-α (IC de 95%: 77.7-117.0) [HR = 0.821 (IC de 95%: 0.673-1.001); p = 0.0510 por prueba de rango logarítmico, p = 0.013 por prueba Wilcoxon] En el análisis estratificado (DHL> contra ≤ 1.5 x LSN, estado de desempeño ECOG 0 contra ≥1, en ausencia o presencia de nefrectomía previa), el HR fue 0.818 (IC de 95%: 0.699 a 0.999; p = 0.049 por prueba de rango logarítmico). La mediana de SG para el grupo IFN-α incluye 25 pacientes que descontinuaron el tratamiento IFN-α debido a progresión de enfermedad y cruzaron a tratamiento con sunitinib. Después de la descontinuación del estudio, 213 pacientes en el grupo IFN-α recibieron un tratamiento de cáncer posterior al estudio, incluyendo a incluyendo a 32% que recibieron sunitinib; 182 pacientes del grupo de sunitinib recibieron tratamiento para el cáncer después del estudio, incluyendo a 11% que recibieron sunitinib. En análisis posthoc los pacientes censurados que pasaron del tratamiento de IFN-α al tratamiento de sunitinib al momento del cambio, la mediana SG fue 114.6 contra 86.7 semanas (rango de riesgo no estratificado: 0.808; p = 0.0361 por prueba de rango logarítmico; p = 0.0081 por prueba Wilcoxon). Cuando se excluyeron los pacientes que recibieron terapias anticáncer posestudio, la mediana de SG fue 121.9 contra 61.3 semanas en sunitinib contra IFN-α respectivamente (HR: 0.647; IC de 95%: 0.482 a 0.867; p = 0.0033 por prueba de rango logarítmico; p = 0.0013 por prueba Wilcoxon).
Tabla 3. Resultados de eficacia CCRm
| Parámetro de eficacia | Primer tratamiento para CCRm |
| Sunitinib (n = 375) | IFN-α (n = 375) | Valor P (prueba de rango logarítmico) | HR (95% CI) |
| Supervivencia libre de progresión [mediana, semanas (IC 95%)] | 48.3 (46.4, 58.3) | 22.1 (17.1, 24.0) | < 0.000001 | 0.516 (0.419, 0.635) |
| Tiempo para progresión del tumor [mediana, semanas (CI de 95%)] | 49.1 (46.6, 59.1) | 22.4 (21.9, 31.3) | < 0.0001 | 0.516 (0.419, (0.635) |
Tasa de respuesta objetivaa
[% (IC95%)] | 38.7 (33.7, 43.8) | 7.7 (5.2,10.9) | < 0.0001 | NA |
| Parámetro de eficacia | CRM refractario a citocinas |
| Estudio 1 (n = 106) | Estudio 2 (n = 63) |
| Tasa de respuesta objetivaa [% (IC95%)] | 34.0a (25.0, 43.8) | 36.5b (24.7, 49.6) |
Duración de la respuesta
[mediana, semanas (IC95%)] | * (42.0,**) | 54b (34.3, 70.1) |
CI= Intervalo de confianza, NA = No aplica.
* La Mediana DR no se ha alcanzado todavía.
** Los datos no son suficientemente maduros para determinar el límite superior de confianza.
a Evaluado por laboratorio central de radiología cegado: el escaneo de 90 pacientes no se había leído al momento del análisis.
b Evaluado por investigadores.
Figura 1. Curva Kaplan-Meier de SLP en estudio de primer tratamiento para CCRm (Población con intención de tratar)
Figura 2. Curva Kaplan-Meier para SG en estudio de tratamiento inicial CCRm (Población con intención de tratar)
Los resultados clínicos reportados por los pacientes fueron medidos utilizando “Functional Assessment of Cancer Therapy -Advanced Kidney Cancer Symptom Index” (FKSI - evaluación funcional de la terapia para el cáncer - índice de síntomas avanzados de cáncer de riñón) y functional assessment of cancer therapy-general (FACT-G - evaluación funcional de la terapia para el cáncer - general). Los criterios de valoración de los resultados reportados de pacientes (RRP) incluyen la calificación FKSI, es la calificación en la subescala de síntomas relacionados con la enfermedad (FKSI - DRS, por sus siglas en inglés), la calificación total de FACT-G y sus cuatro calificaciones de subescala bienestar físico (PWB - Physical Well Being), bienestar social/familiar (SWB - social/family Well Being), bienestar emocional (EWB - emocional well being) y bienestar funcional (FWB - funcional well being). La FKSI-DRS fue previamente especificada como el criterio de valoración primario RRP y se utilizó para evaluar los síntomas relacionados con cáncer de riñón reportados por el paciente (falta de energía, fatiga, dolor/dolor en huesos, pérdida de peso, falta de aire, tos, fiebre y hematuria) en 719 pacientes. Los pacientes tratados con sunitinib reportaron calificaciones del índice FKSI-DRS estadística y significativamente mejores (p ≤ 0.0071), calificaciones FKSI (p ≤ 0.0133), calificaciones totales FACT-G (p≤ 0.0244), bienestar físico (p ≤ 0.0208), y calificaciones de bienestar físico (p ≤ 0.0044) que los pacientes tratados con IFN-α en todos los tiempos de evaluación poslínea basal hasta 20 ciclos por tratamiento. Para el bienestar físico, el bienestar social/familiar, y el bienestar emocional, el nivel de significancia estadística se incrementó por arriba del nivel 0.05 después del ciclo 13, ciclo 15 día 1 y ciclo 10, respectivamente. Comparado con las diferencias importantes mínimas clínicamente preestablecidas para estos criterios de valoración, las diferencias entre los tratamientos para síntomas relacionados al cáncer de riñón (FKSI en todos los puntos de tiempo de poslínea basal y FKSI-DRS después del ciclo 3, día 1) y la calidad de vida en general (FACT-G) en todos los puntos de tiempo de poslínea basal fueron considerados clínicamente significativos.
CCRm refractario a citocinas: Un estudio fase 2 de sunitinib fue realizado en pacientes que fueron refractarios a la terapia anterior de citocina con interleukin-2 o IFN-α. Sesenta y tres pacientes recibieron una dosis inicial de 50 mg de sunitinib oral, una vez al día en el programa 4/2 (n = 63). El criterio de valoración primario de eficacia fue el índice de respuesta objetiva (IRO) con base en el criterio de evaluación de respuesta en tumores sólidos (RECIST – por sus siglas en inglés: response evaluation criteria in solid tumors). Los criterios de valoración secundarios incluyeron la evaluación de TTP, SLP, duración de la respuesta (DR) y SG. En este estudio, el IRO fue 36.5% (CI de 95% = 24.7% - 49.6%), la mediana TTP y SLP fue de 37.7 semanas (IC de 95% = 24.0 – 46.4 semanas).
Un estudio de confirmación, abierto, de un solo grupo y multicéntrico que evalúa la eficacia y seguridad de sunitinib fue realizado en pacientes con CCRm quienes fueron refractarios a la terapia previa con citocinas. Ciento seis pacientes recibieron al menos una dosis de 50 mg de sunitinib en programa 4/2 (n = 106). El criterio de valoración primario de eficacia del estudio fue IRO. Los criterios de valoración secundarios incluyeron Tiempo a la progresión del tumor (TTP), supervivencia libre de progresión (SLP), DR y SG. En este estudio el IRO fue de 34.0% (IC de 95% = 25.0% - 43.8%). La mediana de TTP, SLP, DR y SG aún no se han alcanzado.




