JARDIANCE 25 MG COMPRIMIDOS RECUBIERTOS CON PELICULA
| ATC: Empagliflozina |
| PA: Empagliflozina |
| EXC: Lactosa monohidrato y otros. |
Envases
2. - COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
3. - FORMA FARMACÉUTICA
4. - DATOS CLÍNICOS
5. - PROPIEDADES FARMACOLÓGICAS
6. - DATOS FARMACÉUTICOS
7. - TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
8. - NÚMERO(S) DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
9. - FECHA DE LA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
10. - FECHA DE LA REVISIÓN DEL TEXTO
 1. - NOMBRE DEL MEDICAMENTO
1. - NOMBRE DEL MEDICAMENTO
JARDIANCE 25 mg Comp. recub. con película
 2. - COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
2. - COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Jardiance 10 mg comprimidos recubiertos con película
Cada comprimido contiene 10 mg de empagliflozina.
Excipientes con efecto conocido
Cada comprimido contiene lactosa monohidrato, equivalente a 154,3 mg de lactosa anhidra. Jardiance 25 mg comprimidos recubiertos con película
Cada comprimido contiene 25 mg de empagliflozina.
Excipientes con efecto conocido
Cada comprimido contiene lactosa monohidrato, equivalente a 107,4 mg de lactosa anhidra.
Para consultar la lista completa de excipientes, ver sección 6.1.
 3. - FORMA FARMACÉUTICA
3. - FORMA FARMACÉUTICA
Comprimido recubierto con película (comprimido).
Jardiance 10 mg comprimidos recubiertos con película
Comprimido recubierto con película de color amarillo pálido, redondo, biconvexo, con borde biselado, grabado con la inscripción «S10» en una cara y el logotipo de Boehringer Ingelheim en la otra (diámetro del comprimido: 9,1 mm).
Jardiance 25 mg comprimidos recubiertos con película
Comprimido recubierto con película de color amarillo pálido, ovalado, biconvexo, grabado con la inscripción «S25» en una cara y el logotipo de Boehringer Ingelheim en la otra (longitud del comprimido: 11,1 mm, anchura del comprimido: 5,6 mm).
 4. - DATOS CLÍNICOS
4. - DATOS CLÍNICOS
 4.1 - Indicaciones Terapéuticas de JARDIANCE 25 mg Comp. recub. con película
4.1 - Indicaciones Terapéuticas de JARDIANCE 25 mg Comp. recub. con película
Diabetes mellitus tipo 2
Jardiance está indicado en adultos y niños a partir de 10 años de edad para el tratamiento de la diabetes mellitus tipo 2 no suficientemente controlada asociado a dieta y ejercicio
- - en monoterapia cuando metformina no se considera apropiada debido a intolerancia
- - añadido a otros medicamentos para el tratamiento de la diabetes
Para consultar los resultados de los ensayos respecto a las combinaciones de tratamientos, los efectos en control glucémico y los acontecimientos cardiovasculares y renales, así como las poblaciones estudiadas, ver las secciones 4.4, 4.5 y 5.1.
Insuficiencia cardíaca
Jardiance está indicado en adultos para el tratamiento de la insuficiencia cardíaca crónica sintomática.
Enfermedad renal crónica
Jardiance está indicado en adultos para el tratamiento de la enfermedad renal crónica.
 4.2 - Posología y administración de JARDIANCE 25 mg Comp. recub. con película
4.2 - Posología y administración de JARDIANCE 25 mg Comp. recub. con película
 4.3 - Contraindicaciones de JARDIANCE 25 mg Comp. recub. con película
4.3 - Contraindicaciones de JARDIANCE 25 mg Comp. recub. con película
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
 4.4 - Advertencias y Precauciones de JARDIANCE 25 mg Comp. recub. con película
4.4 - Advertencias y Precauciones de JARDIANCE 25 mg Comp. recub. con película
Generales
Empagliflozina no se debe usar en pacientes con diabetes mellitus tipo 1 (ver “Cetoacidosis” en la sección 4.4).
Cetoacidosis
Se han notificado casos de cetoacidosis, incluidos casos potencialmente mortales y con desenlace mortal, en pacientes con diabetes mellitus tratados con inhibidores del SGLT2, incluida empagliflozina. En algunos de estos casos, la presentación del cuadro clínico fue atípico, con un ascenso moderado en los valores de glucosa en sangre, por debajo de 14 mmol/l (250 mg/dl). Se desconoce si la cetoacidosis puede ocurrir con mayor probabilidad con dosis mayores de empagliflozina. Aunque es menos probable que se produzcan casos de cetoacidosis en pacientes sin diabetes mellitus, también se han notificado casos en estos pacientes.
El riesgo de cetoacidosis se debe considerar en caso de síntomas inespecíficos como náuseas, vómitos, anorexia, dolor abdominal, sed excesiva, dificultad para respirar, confusión, fatiga o somnolencia inusuales. Se debe evaluar a los pacientes de forma inmediata para detectar la cetoacidosis en caso que aparezcan estos síntomas, independientemente del nivel de glucosa en sangre.
En pacientes en los que se sospeche o diagnostique cetoacidosis, el tratamiento con empagliflozina se debe suspender inmediatamente.
Se debe interrumpir el tratamiento en pacientes que están hospitalizados por un procedimiento quirúrgico mayor o enfermedades agudas graves. Se recomienda controlar las cetonas en estos pacientes. Se prefiere la determinación de los niveles de cuerpos cetónicos en sangre a la determinación en orina. El tratamiento con empagliflozina se puede reanudar cuando los valores de cuerpos cetónicos sean normales y el estado del paciente se haya estabilizado.
Antes de iniciar empagliflozina, se deben considerar los antecedentes del paciente que puedan predisponer a cetoacidosis.
Los pacientes que pueden tener un riesgo mayor de cetoacidosis son aquellos pacientes con una baja reserva de células beta funcionales (p. ej., pacientes con diabetes tipo 2 con péptido C bajo o con diabetes autoinmune latente del adulto (LADA) o pacientes con antecedentes de pancreatitis), pacientes con trastornos que den lugar a una ingesta restringida de alimentos o a una deshidratación grave, pacientes cuyas dosis de insulina estén reducidas y pacientes con mayores necesidades de insulina debido a una enfermedad médica aguda, cirugía o abuso de alcohol. Los inhibidores del SGLT2 se deben usar con precaución en estos pacientes.
No se recomienda reiniciar el tratamiento con un inhibidor del SGLT2 en pacientes con cetoacidosis previa mientras estaban en tratamiento con un inhibidor del SGLT2, a menos que se haya identificado y resuelto claramente otro factor desencadenante.
Jardiance no se debe utilizar en pacientes con diabetes tipo 1. Los datos de un programa de ensayos clínicos en pacientes con diabetes tipo 1 mostraron un aumento de la incidencia de cetoacidosis con una frecuencia frecuente en pacientes tratados con 10 mg y 25 mg de empagliflozina como tratamiento complementario de insulina en comparación con un placebo.
Insuficiencia renal
Debido a que la experiencia es limitada, no se recomienda iniciar el tratamiento con empagliflozina en pacientes con una TFGe < 20 ml/min/1,73 m2.
En pacientes con una TFG < 60 ml/min/1,73 m2, la dosis diaria de empagliflozina es 10 mg (ver sección 4.2).
La eficacia hipoglucemiante de empagliflozina depende de la función renal y es menor en pacientes con una TFGe < 45 ml/min/1,73 m2 y probablemente esté ausente en pacientes con una TFGe < 30 ml/min/1,73 m2 (ver las secciones 4.2, 5.1 y 5.2).
Monitorización de la función renal
Se recomienda evaluar la función renal tal como se indica a continuación:
- - Antes de iniciar el tratamiento con empagliflozina y periódicamente durante el tratamiento, al menos una vez al año (ver las secciones 4.2, 4.8, 5.1 y 5.2).
- - Antes de iniciar el tratamiento con cualquier medicamento concomitante que pueda tener un impacto negativo en la función renal.
Riesgo de hipovolemia
En base al modo de acción de los inhibidores del SGLT2, la diuresis osmótica que acompaña a la glucosuria puede provocar una disminución moderada de la presión arterial (ver sección 5.1). Por lo tanto, se debe tener precaución en los pacientes para los que una caída de la presión arterial inducida por empagliflozina pudiera suponer un riesgo, tales como pacientes con enfermedad cardiovascular conocida, pacientes en tratamiento antihipertensivo con antecedentes de hipotensión o pacientes de 75 años de edad o mayores.
En caso de enfermedades que puedan conducir a una pérdida de líquidos (por ejemplo, una enfermedad gastrointestinal), se recomienda una estrecha monitorización de la volemia (por ejemplo, exploración física, medición de la presión arterial, pruebas de laboratorio, incluyendo el hematocrito) y de los electrolitos en el caso de pacientes que reciben empagliflozina. Se debe valorar la interrupción temporal del tratamiento con empagliflozina hasta que se corrija la pérdida de líquidos.
Pacientes de edad avanzada
El efecto de empagliflozina en la eliminación de glucosa por la orina se asocia a la diuresis osmótica, lo que podría afectar al estado de hidratación. Los pacientes de 75 años de edad o mayores pueden presentar un mayor riesgo de hipovolemia. Un mayor número de estos pacientes tuvieron reacciones adversas relacionadas con la hipovolemia en comparación con los tratados con placebo (ver sección 4.8). Por tanto, se debe prestar especial atención a la ingesta de líquidos en caso de que se administre de forma conjunta con medicamentos que puedan producir hipovolemia (p. ej., diuréticos, inhibidores de la ECA).
Infecciones complicadas del tracto urinario
Se han notificado casos de infecciones complicadas del tracto urinario incluyendo pielonefritis y urosepsis en pacientes tratados con empagliflozina (ver sección 4.8). En el caso de pacientes con infecciones complicadas del tracto urinario, debe valorarse la interrupción temporal del tratamiento con empagliflozina.
Fascitis necrosante del perineo (gangrena de Fournier)
Se han notificado casos de fascitis necrosante del perineo (también conocida como gangrena de Fournier) en pacientes de ambos sexos con diabetes mellitus tratados con inhibidores del SGLT2. Se trata de un acontecimiento raro pero grave y potencialmente mortal que requiere intervención quirúrgica urgente y tratamiento antibiótico.
Se indicará a los pacientes que acudan al médico si presentan una combinación de síntomas como dolor, dolor a la palpación, eritema o inflamación en la región genital o perineal, con fiebre o malestar general. Tenga en cuenta que la infección urogenital o el absceso perineal pueden preceder a la fascitis necrosante. Si se sospecha gangrena de Fournier, se debe interrumpir Jardiance e instaurar un tratamiento inmediato (incluidos antibióticos y desbridamiento quirúrgico).
Amputaciones de miembros inferiores
Se ha observado un incremento en los casos de amputación de miembros inferiores (principalmente de los dedos de los pies) en ensayos clínicos a largo plazo con otro inhibidor de SGLT2. Se desconoce si esto constituye un efecto de clase. Al igual que para todos los pacientes diabéticos, es importante aconsejar a los pacientes acerca del cuidado rutinario preventivo de los pies.
Lesión hepática
Se han notificado casos de lesión hepática con el uso de empagliflozina en ensayos clínicos. No se ha establecido una relación causal entre empagliflozina y la lesión hepática.
Aumento del hematocrito
Se ha observado un aumento del hematocrito con el tratamiento con empagliflozina (ver sección 4.8).
Enfermedad renal crónica
Los pacientes con albuminuria pueden beneficiarse más del tratamiento con empagliflozina.
Enfermedad infiltrativa o miocardiopatía de Takotsubo
No se ha estudiado específicamente a pacientes con enfermedad infiltrativa o con miocardiopatía de Takotsubo. Por consiguiente, no se ha establecido la eficacia en estos pacientes.
Análisis de orina
Debido a su mecanismo de acción, los pacientes que están tomando Jardiance presentarán un resultado positivo para la glucosa en la orina.
Interferencia con la prueba del 1,5-anhidroglucitol (1,5-AG)
No se recomienda la monitorización del control de la glucemia con la prueba del 1,5-AG, ya que las mediciones de 1,5-AG no son fiables para valorar el control de la glucemia en pacientes que toman inhibidores del SGLT2. Se recomienda el uso de métodos alternativos para la monitorización del control de la glucemia.
Lactosa
Los comprimidos contienen lactosa. Los pacientes con intolerancia hereditaria a galactosa, deficiencia total de lactasa o problemas de absorción de glucosa o galactosa no deben tomar este medicamento.
Sodio
Cada comprimido contiene menos de 1 mmol de sodio (23 mg); esto es, esencialmente “exento de sodio”.
 4.5 - Interacciones con otros medicamentos de JARDIANCE 25 mg Comp. recub. con película
4.5 - Interacciones con otros medicamentos de JARDIANCE 25 mg Comp. recub. con película
Interacciones farmacodinámicas
Diuréticos
Empagliflozina puede aumentar el efecto diurético de las tiazidas y de los diuréticos del asa y puede aumentar el riesgo de deshidratación e hipotensión (ver sección 4.4).
Insulina y secretagogos de insulina
La insulina y los secretagogos de insulina, como las sulfonilureas, pueden aumentar el riesgo de hipoglucemia. Por lo tanto, puede necesitarse una dosis más baja de insulina o de un secretagogo de insulina para disminuir el riesgo de hipoglucemia cuando éstos se usan en combinación con empagliflozina (ver las secciones 4.2 y 4.8).
Interacciones farmacocinéticas
Efectos de otros medicamentos sobre empagliflozina
Los datos in vitro sugieren que la principal vía metabólica de empagliflozina en humanos es la glucuronidación por las uridina 5'-difosfoglucuronosiltransferasas UGT1A3, UGT1A8, UGT1A9 y UGT2B7. Empagliflozina es un sustrato de los transportadores de captación humanos OAT3, OATP1B1, y OATP1B3, pero no de OAT1 y OCT2. Empagliflozina es un sustrato de la glicoproteína-P (gp-P) y la proteína de resistencia al cáncer de mama (BCRP).
La administración conjunta de empagliflozina con probenecid, un inhibidor de las enzimas UGT y del OAT3, dio lugar a un aumento del 26 % en las concentraciones plasmáticas máximas (Cmax) de empagliflozina y a un aumento del 53 % en el área bajo la curva concentración-tiempo (AUC). Estos cambios no se consideraron clínicamente significativos.
No se ha estudiado el efecto de la inducción de la UGT (p. ej., inducción por rifampicina o por fenitoína) sobre empagliflozina. No se recomienda el tratamiento concomitante con inductores de las enzimas UGT debido al riesgo potencial de que disminuya la eficacia. Si se debe administrar de forma concomitante un inductor de estas enzimas UGT, se recomienda vigilar el control de la glucemia para determinar que la respuesta a Jardiance es adecuada.
Un estudio de interacción con gemfibrozilo, un inhibidor in vitro de los transportadores OAT3 y OATP1B1/1B3, mostró que la Cmax de empagliflozina aumentaba en un 15 % y el AUC aumentaba en un 59 % después de la administración conjunta. Estos cambios no se consideraron clínicamente significativos.
La inhibición de los transportadores OATP1B1/1B3 mediante la administración conjunta de rifampicina dio lugar a un aumento del 75 % en la Cmax y un aumento del 35 % en el AUC de empagliflozina. Estos cambios no se consideraron clínicamente significativos.
La exposición a empagliflozina fue similar con y sin la administración conjunta de verapamilo, un inhibidor de la gp-P, lo que indica que la inhibición de la gp-P no tiene un efecto clínicamente relevante sobre empagliflozina.
Los estudios de interacciones sugieren que la farmacocinética de empagliflozina no se vio influida por la administración conjunta de metformina, glimepirida, pioglitazona, sitagliptina, linagliptina, warfarina, verapamilo, ramipril, simvastatina, torasemida e hidroclorotiazida.
Efectos de empagliflozina sobre otros medicamentos
Empagliflozina puede aumentar la excreción renal de litio y reducir así los niveles sanguíneos de litio. Se debe monitorizar la concentración sérica de litio con mayor frecuencia después del inicio del tratamiento y de los cambios de dosis de empagliflozina. Derive al paciente al médico que le prescribió litio para que le monitorice la concentración sérica de litio.
En base a los estudios in vitro, empagliflozina no inhibe, inactiva ni induce las isoformas del CYP450. Empagliflozina no inhibe la UGT1A1, la UGT1A3, la UGT1A8, la UGT1A9 ni la UGT2B7. Por lo tanto, se considera improbable que se produzcan interacciones farmacológicas que impliquen a las principales isoformas del CYP450 y de la UGT con empagliflozina y a los sustratos de estas enzimas administrados de forma conjunta.
Empagliflozina no inhibe la gp-P a dosis terapéuticas. En base a los estudios in vitro, se considera improbable que empagliflozina provoque interacciones con principios activos que sean sustratos de la gp-P. La administración conjunta de digoxina, un sustrato de la gp-P, con empagliflozina dio lugar a un aumento del 6 % en el AUC y un aumento del 14 % en la Cmax de la digoxina. Estos cambios no se consideraron clínicamente significativos.
Empagliflozina no inhibe in vitro a los transportadores de captación humanos, tales como OAT3, OATP1B1 y OATP1B3 a concentraciones plasmáticas clínicamente relevantes y, como tales, las interacciones farmacológicas con sustratos de estos transportadores de captación se consideran improbables.
Los estudios de interacciones realizados en voluntarios sanos sugieren que empagliflozina no tuvo ningún efecto clínicamente relevante sobre la farmacocinética de metformina, glimepirida, pioglitazona, sitagliptina, linagliptina, simvastatina, warfarina, ramipril, digoxina, diuréticos y anticonceptivos orales.
Población pediátrica
Los estudios de interacciones se han realizado solo en adultos.
 4.6 - Embarazo y Lactancia de JARDIANCE 25 mg Comp. recub. con película
4.6 - Embarazo y Lactancia de JARDIANCE 25 mg Comp. recub. con película
Embarazo
No hay datos sobre el uso de empagliflozina en mujeres embarazadas. Los estudios realizados en animales muestran que empagliflozina atraviesa la placenta durante la última fase de la gestación en un grado muy limitado, pero no indican efectos perjudiciales directos ni indirectos en lo que respecta al desarrollo embrionario temprano. No obstante, los estudios realizados en animales han mostrado efectos adversos en el desarrollo posnatal (ver sección 5.3). Como medida de precaución, es preferible evitar el uso de Jardiance durante el embarazo.
Lactancia
No se dispone de datos en humanos sobre la excreción de empagliflozina en la leche materna. Los datos toxicológicos disponibles en animales han mostrado que empagliflozina se excreta en la leche. No se puede excluir el riesgo para los recién nacidos o los lactantes. Jardiance no debe utilizarse durante la lactancia.
Fertilidad
No se han realizado estudios sobre el efecto de Jardiance en la fertilidad humana. Los estudios realizados en animales no sugieren efectos perjudiciales directos o indirectos sobre la fertilidad (ver sección 5.3).
 4.7 - Efectos sobre la capacidad de conducción de JARDIANCE 25 mg Comp. recub. con película
4.7 - Efectos sobre la capacidad de conducción de JARDIANCE 25 mg Comp. recub. con película
La influencia de Jardiance sobre la capacidad para conducir y utilizar máquinas es pequeña. Se debe advertir a los pacientes que tomen las debidas precauciones para evitar una hipoglucemia mientras conducen y utilizan máquinas, sobre todo cuando Jardiance se use en combinación con una sulfonilurea y/o con insulina.
 4.8 - Reacciones Adversas de JARDIANCE 25 mg Comp. recub. con película
4.8 - Reacciones Adversas de JARDIANCE 25 mg Comp. recub. con película
Resumen del perfil de seguridad
Diabetes mellitus tipo 2
Se incluyeron un total de 15 582 pacientes con diabetes tipo 2 en ensayos clínicos para evaluar la seguridad de empagliflozina, de los cuales, 10 004 pacientes recibieron empagliflozina, ya sea como monoterapia o en combinación con metformina, una sulfonilurea, pioglitazona, inhibidores de la DPP-4 o insulina.
En 6 ensayos controlados con placebo de 18 a 24 semanas de duración, se incluyeron 3 534 pacientes, de los cuales, 1 183 se trataron con placebo y 2 351 con empagliflozina. La incidencia global de reacciones adversas en pacientes tratados con empagliflozina fue similar a la de los tratados con placebo. La reacción adversa notificada con más frecuencia fue la hipoglucemia cuando se usó con una sulfonilurea o con insulina (ver la descripción de las reacciones adversas seleccionadas).
Insuficiencia cardíaca
Los estudios EMPEROR incluyeron a pacientes con insuficiencia cardíaca y fracción de eyección reducida (N = 3 726) o fracción de eyección preservada (N = 5 985) tratados con 10 mg de empagliflozina o con un placebo. Aproximadamente la mitad de los pacientes tenía diabetes mellitus tipo 2. La reacción adversa más frecuente de los estudios EMPEROR-Reduced y EMPEROR-Preserved agrupados fue hipovolemia (empagliflozina 10 mg: 11,4 %; placebo: 9,7 %).
Enfermedad renal crónica
El estudio EMPA-KIDNEY incluyó a pacientes con enfermedad renal crónica (N = 6 609) tratados con 10 mg de empagliflozina o con un placebo. Aproximadamente el 44 % de los pacientes tenía diabetes mellitus tipo 2. Los acontecimientos adversos más frecuentes en el estudio EMPA-KIDNEY fueron gota (7,0 % con empagliflozina frente a 8,0 % con placebo) y fracaso renal agudo (2,8 % con empagliflozina frente a 3,5 % con placebo), que se notificaron con mayor frecuencia en los pacientes tratados con el placebo.
El perfil de seguridad global de empagliflozina fue generalmente homogéneo en las indicaciones estudiadas.
Tabla de reacciones adversas
En la tabla siguiente (Tabla 1) se presentan las reacciones adversas notificadas en pacientes que recibieron empagliflozina en estudios controlados con placebo, según la clasificación por órganos y sistemas y los términos preferentes de MedDRA.
Las reacciones adversas se incluyen según la frecuencia absoluta. Las frecuencias se definen como muy frecuentes (≥1/10), frecuentes (≥1/100 a <1/10), poco frecuentes (≥1/1 000 a <1/100), raras (≥1/10 000 a <1/1 000), muy raras (<1/10 000) y frecuencia no conocida (no puede estimarse a partir de los datos disponibles).
Tabla 1: Tabla de reacciones adversas (MedDRA) procedentes de los ensayos controlados con placebo y de la experiencia poscomercialización
| Clasificación por Órganos y Sistemas | Muy frecuentes | Frecuentes | Poco frecuentes | Raras | Muy raras |
| Infecciones e infestaciones | Moniliasis vaginal, vulvovaginitis, balanitis y otras infecciones genitalesa Infección del tracto urinario (incluyendo pielonefritis y urosepsis)a | Fascitis necrosante del perineo (gangrena de Fournier)* | |||
| Trastornos del metabolismo y de la nutrición | Hipoglucemia (cuando se usa con una sulfonilurea o con insulina)a | Sed | Cetoacidosis * | ||
| Trastornos gastrointestinales | Estreñimiento | ||||
| Trastornos de la piel y del tejido subcutáneo | Prurito (generalizado) Exantema | Urticaria Angioedema | |||
| Trastornos vasculares | Hipovolemiaa | ||||
| Trastornos renales y urinarios | Aumento de la miccióna | Disuria | Nefritis tubulointersticial | ||
| Exploraciones complementarias | Aumento de los lípidos en sueroa | Aumento de la creatinina en sangre/disminución de la tasa de filtración glomerulara Aumento del hematocritoa |
a ver las subsecciones siguientes para obtener información adicional
* ver sección 4.4
Descripción de reacciones adversas seleccionadas
Hipoglucemia
La frecuencia de hipoglucemia dependió del tratamiento de base utilizado en los estudios y fue similar para empagliflozina y placebo en monoterapia, tratamiento de adición a metformina, tratamiento de adición a pioglitazona con o sin metformina, como tratamiento de adición a linagliptina y metformina y como asociado al tratamiento de referencia para la combinación de empagliflozina con metformina en pacientes sin tratamiento previo en comparación con aquellos tratados con empagliflozina y metformina como componentes individuales. Se observó un aumento de la frecuencia cuando se administró como tratamiento de adición a metformina y una sulfonilurea (empagliflozina 10 mg 16,1 %, empagliflozina 25 mg: 11,5 %, placebo: 8,4 %), como tratamiento de adición a insulina basal con o sin metformina y con o sin sulfonilurea (empagliflozina 10 mg: 19,5 %, empagliflozina 25 mg: 28,4 %, placebo: 20,6 % durante las 18 primeras semanas de tratamiento cuando insulina no pudo ajustarse; empagliflozina 10 mg y 25 mg: 36,1 %, placebo 35,3 % a lo largo del ensayo de 78 semanas), y como tratamiento de adición a insulina en inyecciones diarias múltiples con o sin metformina (empagliflozina 10 mg; 39,8 %, empagliflozina 25 mg: 41,3 %, placebo: 37,2 % durante el tratamiento inicial de 18 semanas cuando no se pudo ajustar insulina; empagliflozina 10 mg: 51,1 %, empagliflozina 25 mg: 57,7 %, placebo: 58 % durante el ensayo de 52 semanas).
En los estudios de insuficiencia cardíaca EMPEROR, se observó una frecuencia similar de hipoglucemia cuando se utilizó como tratamiento de adición a una sulfonilurea o a insulina (empagliflozina 10 mg: 6,5 %; placebo: 6,7 %).
Hipoglucemia grave (acontecimientos que requieran asistencia)
No se observó ningún aumento en la hipoglucemia grave con el uso de empagliflozina en comparación con el placebo en monoterapia, tratamiento de adición a metformina, tratamiento de adición a metformina y una sulfonilurea, tratamiento de adición a pioglitazona con o sin metformina, tratamiento de adición a linagliptina y metformina, asociado al tratamiento de referencia y para la combinación de empagliflozina con metformina en pacientes sin tratamiento previo en comparación con aquellos tratados con empagliflozina y metformina como componentes individuales. Se observó un aumento de la frecuencia cuando se administró como tratamiento de adición a insulina basal con o sin metformina y con o sin una sulfonilurea (empagliflozina 10 mg: 0 %, empagliflozina 25 mg 1,3 %, placebo: 0 % durante las 18 primeras semanas de tratamiento cuando insulina no pudo ajustarse; empagliflozina 10 mg: 0 %, empagliflozina 25 mg: 1,3 %, placebo 0 % a lo largo del ensayo de 78 semanas) y tratamiento de adición a insulina en inyecciones diarias múltiples con o sin metformina (empagliflozina 10 mg: 0,5 %, empagliflozina 25 mg: 0,5 %, placebo: 0,5 % durante el tratamiento inicial de 18 semanas cuando no se pudo ajustar insulina; empagliflozina 10 mg: 1,6 %, empagliflozina 25 mg: 0,5 %, placebo: 1,6 % durante el ensayo de 52 semanas).
En los estudios de insuficiencia cardíaca EMPEROR, se observó hipoglucemia grave con frecuencias similares en los pacientes con diabetes mellitus tratados con empagliflozina y con placebo como tratamiento de adición a una sulfonilurea o a insulina (empagliflozina 10 mg: 2,2 %; placebo: 1,9 %).
Moniliasis vaginal, vulvovaginitis, balanitis y otras infecciones genitales
La moniliasis vaginal, la vulvovaginitis, la balanitis y otras infecciones genitales se notificaron con más frecuencia en los pacientes tratados con empagliflozina (empagliflozina 10 mg: 4,0 %, empagliflozina 25 mg: 3,9 %) en comparación con placebo (1,0 %). Estas infecciones se notificaron con más frecuencia en mujeres tratadas con empagliflozina en comparación con placebo, y la diferencia en cuanto a frecuencia fue menos pronunciada en el caso de los hombres. Las infecciones del tracto genital fueron de intensidad leve a moderada.
En los estudios de insuficiencia cardíaca EMPEROR, la frecuencia de estas infecciones fue más pronunciada en los pacientes con diabetes mellitus (empagliflozina 10 mg: 2,3 %; placebo: 0,8 %) que en los pacientes sin diabetes mellitus (empagliflozina 10 mg: 1,7 %; placebo: 0,7 %) cuando recibieron tratamiento con empagliflozina en comparación con el placebo.
Aumento de la micción
El aumento de la micción (incluyendo los términos predefinidos polaquiuria, poliuria y nocturia) se observó con mayor frecuencia en los pacientes tratados con empagliflozina (empagliflozina 10 mg: 3,5 %, empagliflozina 25 mg: 3,3 %) en comparación con placebo (1,4 %). El aumento de la micción fue principalmente de intensidad leve a moderada. La frecuencia notificada de nocturia fue similar para placebo y para empagliflozina (<1 %).
En los estudios de insuficiencia cardíaca EMPEROR, se observó un aumento de la micción con frecuencias similares en los pacientes tratados con empagliflozina y con placebo (empagliflozina 10 mg: 0,9 %; placebo 0,5 %).
Infecciones del tracto urinario
La frecuencia global de infecciones del tracto urinario notificadas como reacciones adversas fue similar en los pacientes tratados con empagliflozina 25 mg y con placebo (7,0 % y 7,2 %) y mayor con empagliflozina 10 mg (8,8 %). De manera similar al placebo, las infecciones del tracto urinario se notificaron con más frecuencia para empagliflozina en pacientes con antecedentes de infecciones crónicas o recurrentes del tracto urinario. La intensidad (leve, moderada, grave) de las infecciones del tracto urinario fue similar en pacientes tratados con empagliflozina y con placebo. Las infecciones del tracto urinario se notificaron con más frecuencia en las mujeres tratadas con empagliflozina en comparación con placebo; no hubo diferencia en el caso de los hombres.
Hipovolemia
La frecuencia global de hipovolemia (incluyendo los términos predefinidos disminución (ambulatoria) de la presión arterial, disminución de la presión arterial sistólica, deshidratación, hipotensión, hipovolemia, hipotensión ortostática y síncope) fue similar en los pacientes tratados con empagliflozina (empagliflozina 10 mg: 0,6 %, empagliflozina 25 mg: 0,4 %) y con placebo (0,3 %).
La frecuencia de acontecimientos de hipovolemia fue mayor en los pacientes de 75 años de edad o mayores, tratados con empagliflozina 10 mg (2,3 %) o empagliflozina 25 mg (4,3 %) en comparación con placebo (2,1 %).
Aumento de la creatinina en sangre/Disminución de la tasa de filtración glomerular
La frecuencia general de pacientes con aumento de la creatinina en sangre y disminución de la tasa de filtración glomerular fue similar entre empaglifozina y placebo (aumento de la creatinina en sangre: empagliflozina 10 mg 0,6 %, empagliflozina 25 mg 0,1 %, placebo 0,5 %; disminución de tasa de la filtración glomerular: empagliflozina 10 mg 0,1 %, empagliflozina 25 mg 0 %, placebo 0,3 %).
Por lo general, los aumentos iniciales en la creatinina y las disminuciones iniciales en la tasa de filtración glomerular estimada en los pacientes tratados con empaglifozina fueron transitorios durante el tratamiento continuo o reversibles tras la suspensión del tratamiento con el medicamento.
De manera uniforme, en el ensayo EMPA-REG OUTCOME, los pacientes tratados con empagliflozina experimentaron un descenso inicial de la TFGe (media: 3 ml/min/1,73 m2). Posteriormente, la TFGe se mantuvo durante la continuación del tratamiento. La TFGe media recuperó el nivel basal tras la suspensión del tratamiento, lo cual indica que en estos cambios de la función renal podrían estar implicados cambios hemodinámicos agudos. Este fenómeno también se observó en los estudios de insuficiencia cardíaca EMPEROR y en el estudio EMPA-KIDNEY.
Aumento de los lípidos séricos
Los aumentos porcentuales medios con respecto al valor inicial para empagliflozina 10 mg y 25 mg en comparación con placebo, respectivamente, fueron: colesterol total, 4,9 % y 5,7 % frente a 3,5 %; colesterol-HDL, 3,3 % y 3,6 % frente a 0,4 %; colesterol-LDL, 9,5 % y 10,0 % frente a 7,5 %; triglicéridos, 9,2 % y 9,9 % frente a 10,5 %.
Aumento del hematocrito
Los cambios medios del hematocrito con respecto al valor inicial fueron del 3,4 % y 3,6 % para empagliflozina 10 mg y 25 mg, respectivamente, en comparación con el 0,1 % para el placebo. En el estudio EMPA-REG Outcome, el hematocrito retornó hacia los valores iniciales después de un periodo de seguimiento de 30 días tras la interrupción del tratamiento.
Población pediátrica
En el ensayo DINAMO se trataron 157 niños de 10 años de edad o mayores con diabetes tipo 2, de los cuales 52 pacientes recibieron empagliflozina, 52 recibieron linagliptina y 53 recibieron placebo (ver sección 5.1).
Durante la fase controlada con placebo, la reacción adversa más frecuente fue la hipoglucemia, con tasas globales más altas en los pacientes tratados con empagliflozina agrupados que en los tratados con placebo (empagliflozina 10 mg y 25 mg, datos agrupados: 23,1 %; placebo: 9,4 %). Ninguna de estas reacciones fue grave ni precisó asistencia.
En general, el perfil de seguridad en niños fue similar al perfil de seguridad observado en adultos con diatebes mellitus tipo 2.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es.
 4.9 - Sobredosificación de JARDIANCE 25 mg Comp. recub. con película
4.9 - Sobredosificación de JARDIANCE 25 mg Comp. recub. con película
Síntomas
En ensayos clínicos controlados, dosis únicas de hasta 800 mg de empagliflozina en voluntarios sanos y dosis múltiples diarias de hasta 100 mg de empagliflozina en pacientes con diabetes tipo 2 no mostraron toxicidad. Empagliflozina aumentó la excreción de glucosa por la orina, lo que provocó un aumento en el volumen de orina. El aumento observado en el volumen de orina no fue dependiente de la dosis y no es clínicamente significativo. No hay experiencia con dosis superiores a 800 mg en humanos.
Tratamiento
En caso de sobredosis, debe iniciarse un tratamiento adecuado al estado clínico del paciente. No se ha estudiado la eliminación de empagliflozina mediante hemodiálisis.
 5. - PROPIEDADES FARMACOLÓGICAS
5. - PROPIEDADES FARMACOLÓGICAS
 5.1 - Propiedades farmacodinámicas de JARDIANCE 25 mg Comp. recub. con película
5.1 - Propiedades farmacodinámicas de JARDIANCE 25 mg Comp. recub. con película
Grupo farmacoterapéutico: Fármacos usados en la diabetes, Inhibidores del cotransportador de sodio-glucosa de tipo 2 (SGLT2), código ATC: A10BK03
Mecanismo de acción
Empagliflozina es un inhibidor competitivo reversible y selectivo altamente potente (IC50 de 1,3 nmol) del cotransportador de sodio-glucosa tipo 2 (SGLT2). Empagliflozina no inhibe otros transportadores de glucosa importantes para el transporte de glucosa a los tejidos periféricos y es 5 000 veces más selectivo para el SGLT2 que para el SGLT1, el transportador más importante responsable de la absorción de glucosa en el intestino. El SGLT2 se encuentra altamente expresado en el riñón, mientras que la expresión en otros tejidos es inexistente o muy baja. Es responsable, como transportador predominante, de la reabsorción de glucosa tras la filtración glomerular para devolverla a la circulación. En los pacientes con diabetes tipo 2 e hiperglucemia, se filtra y reabsorbe una mayor cantidad de glucosa.
Empagliflozina mejora el control glucémico en pacientes con diabetes tipo 2 al reducir la reabsorción renal de glucosa. La cantidad de glucosa eliminada por el riñón mediante este mecanismo glucurético depende de la concentración de glucosa en sangre y de la TFG. La inhibición del SLGT2 en pacientes con diabetes tipo 2 e hiperglucemia conduce a un exceso de excreción de glucosa por la orina.
Además, el inicio de la administración de empagliflozina aumenta la excreción de sodio, que da lugar a diuresis osmótica y a un volumen intravascular reducido.
En pacientes con diabetes tipo 2, la excreción de glucosa por la orina aumentó inmediatamente después de la primera dosis de empagliflozina y se mantuvo continua durante el intervalo de administración de 24 horas. El aumento en la eliminación de glucosa por la orina se mantuvo al final del periodo de tratamiento de 4 semanas, con un promedio de aproximadamente 78 g/día. El aumento en la eliminación de glucosa por la orina dio lugar a una reducción inmediata de los niveles de glucosa plasmática en pacientes con diabetes tipo 2.
Empagliflozina mejora los niveles de glucosa en plasma, tanto en ayunas como posprandiales. El mecanismo de acción de empagliflozina es independiente de la función de las células beta y de la vía de la insulina, y esto contribuye a un bajo riesgo de hipoglucemia. Se observó una mejora de los marcadores indirectos de la función de las células beta, incluido el Modelo Homeostático β para la evaluación de la resistencia a la insulina (HOMA-β). Además, la excreción de glucosa por la orina desencadena una pérdida de calorías, que se asocia a una pérdida de grasa corporal y a una reducción de peso corporal. La glucosuria observada con empagliflozina se ve acompañada por una diuresis, que puede contribuir a la reducción sostenida y moderada de la presión arterial.
Empagliflozina también reduce la reabsorción de sodio y aumenta la llegada de sodio al túbulo distal. Esto puede influir en diversas funciones fisiológicas tales como, pero no exclusivamente, las siguientes: aumento de la retroalimentación tubuloglomerular y reducción de la presión intraglomerular, reducción de la precarga y la poscarga cardíacas, disminución de la actividad simpática y reducción de la tensión parietal del ventrículo izquierdo manifestada por valores inferiores de NT-proBNP que pueden tener efectos beneficiosos sobre la remodelación cardíaca, las presiones de llenado y la función diastólica, así como sobre la preservación de la estructura y la función renales.
Otros efectos tales como un aumento del hematocrito y una reducción del peso corporal y de la presión arterial también pueden contribuir a los efectos beneficiosos cardíacos y renales.
Eficacia clínica y seguridad
Diabetes mellitus tipo 2
Tanto la mejora del control glucémico como la reducción de la morbilidad y mortalidad cardiovasculares son una parte integral del tratamiento de la diabetes tipo 2.
En 12 ensayos clínicos doble ciego, controlados con placebo y con activo, se ha evaluado la eficacia glucémica y los resultados cardiovasculares en un total de 14 663 pacientes con diabetes tipo 2, de los cuales 9 295 recibieron empagliflozina (empagliflozina 10 mg: 4 165 pacientes; empagliflozina 25 mg: 5 130 pacientes). Cinco estudios tuvieron una duración del tratamiento de 24 semanas; las extensiones de estos y otros estudios incluyeron a pacientes expuestos a empagliflozina hasta un máximo de 102 semanas.
El tratamiento con empagliflozina como monoterapia y en combinación con metformina, pioglitazona, una sulfonilurea, inhibidores de la DPP-4 e insulina proporcionó mejoras clínicamente significativas en HbA1c, glucosa plasmática en ayunas (GPA), peso corporal y presión arterial sistólica y diastólica. Con la administración de empagliflozina 25 mg, una mayor proporción de pacientes logró el objetivo de alcanzar una HbA1c inferior al 7 % y hubo menos pacientes que necesitaron un rescate glucémico en comparación con empagliflozina 10 mg y placebo. Se asoció un nivel basal más alto de HbA1c con una mayor reducción de la HbA1c. Además, empagliflozina asociada al tratamiento de referencia redujo la mortalidad cardiovascular en pacientes con diabetes tipo 2 y enfermedad cardiovascular establecida.
Monoterapia
Se evaluó la eficacia y seguridad de empagliflozina en monoterapia en un ensayo doble ciego controlado con placebo y con activo de 24 semanas de duración, con pacientes que no habían recibido ningún tratamiento anterior. El tratamiento con empagliflozina dio lugar a una reducción estadísticamente significativa (p<0,0001) de HbA1c en comparación con el placebo (Tabla 2), así como a una disminución clínicamente significativa de la GPA.
En un análisis pre-especificado de pacientes (N = 201) con un nivel basal de la HbA1c ≥8,5 %, el tratamiento provocó una reducción de la HbA1c respecto a los valores basales del -1,44 % para empagliflozina 10 mg, del -1,43 % para empagliflozina 25 mg y del -1,04 % para sitagliptina, así como un aumento del 0,01 % para el placebo.
En la extensión doble ciego controlada con placebo de este ensayo, las reducciones en la HbA1c, el peso corporal y la presión arterial se mantuvieron hasta la semana 76.
Tabla 2: Resultados de eficacia de un ensayo controlado con placebo de 24 semanas de duración de empagliflozina como monoterapiaa
| Placebo | Jardiance | Sitagliptina | ||
| 10 mg | 25 mg | 100 mg | ||
| N | 228 | 224 | 224 | 223 |
| HbA1c (%) | ||||
| Valor basal (media) | 7,91 | 7,87 | 7,86 | 7,85 |
| Cambio respecto al valor basal1 | 0,08 | -0,66 | -0,78 | -0,66 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,74* (-0,90, -0,57) | -0,85* (-1,01, -0,69) | -0,73 (-0,88, -0,59)3 | |
| N | 208 | 204 | 202 | 200 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 %2 | 12,0 | 35,3 | 43,6 | 37,5 |
| N | 228 | 224 | 224 | 223 |
| Peso corporal (kg) | ||||
| Valor basal (media) | 78,23 | 78,35 | 77,80 | 79,31 |
| Cambio respecto al valor basal1 | -0,33 | -2,26 | -2,48 | 0,18 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -1,93* (-2,48, -1,38) | -2,15* (-2,70, -1,60) | 0,52 (-0,04, 1,00)3 | |
| N | 228 | 224 | 224 | 223 |
| PAS (mm Hg)4 | ||||
| Valor basal (media) | 130,4 | 133,0 | 129,9 | 132,5 |
| Cambio respecto al valor basal1 | -0,3 | -2,9 | -3,7 | 0,5 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -2,6* (-5,2, -0,0) | -3,4* (-6,0, - 0,9) | 0,8 (-1,4, 3,1)3 | |
a Grupo completo de análisis (FAS) utilizando la última observación considerada (LOCF) antes del tratamiento de rescate glucémico
1 Media ajustada respecto al valor basal
2 No evaluado en cuanto a significación estadística debido al resultado del procedimiento de prueba confirmatorio secuencial
3 IC del 95 %
4 LOCF, valores censurados estadísticamente después del rescate antihipertensivo
*valor p<0,0001
Tratamiento de combinación
Empagliflozina como tratamiento en combinación con metformina, sulfonilurea, pioglitazona
Empagliflozina como tratamiento de adición a metformina, metformina y una sulfonilurea o pioglitazona con o sin metformina dio lugar a reducciones estadísticamente significativas (p<0,0001) en la HbA1c y en el peso corporal en comparación con el placebo (Tabla 3). Además, también dio lugar a una reducción clínicamente significativa en la GPA y la presión arterial sistólica y diastólica en comparación con el placebo.
En la extensión doble ciego controlada con placebo de estos estudios, la reducción en la HbA1c, el peso corporal y la presión arterial se mantuvo hasta la semana 76.
Tabla 3: Resultados de eficacia de los ensayos controlados con placebo de 24 semanasa
| Tratamiento de adición a metformina | |||
| Placebo | Jardiance | ||
| 10 mg | 25 mg | ||
| N | 207 | 217 | 213 |
| HbA1c (%) | |||
| Valor basal (media) | 7,90 | 7,94 | 7,86 |
| Cambio respecto al valor basal1 | -0,13 | -0,70 | -0,77 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,57* (-0,72, -0,42) | -0,64* (-0,79, -0,48) | |
| N | 184 | 199 | 191 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 %2 | 12,5 | 37,7 | 38,7 |
| N | 207 | 217 | 213 |
| Peso corporal (kg) | |||
| Valor basal (media) | 79,73 | 81,59 | 82,21 |
| Cambio respecto al valor basal1 | -0,45 | -2,08 | -2,46 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -1,63* (-2,17, -1,08) | -2,01* (-2,56, -1,46) | |
| N | 207 | 217 | 213 |
| PAS (mm Hg)2 | |||
| Valor basal (media) | 128,6 | 129,6 | 130,0 |
| Cambio respecto al valor basal1 | -0,4 | -4,5 | -5,2 |
| Diferencia respecto al placebo1 (IC del 95 %) | -4,1* (-6,2, -2,1) | -4,8* (-6,9, -2,7) | |
| Tratamiento de adición a metformina y una sulfonilurea | |||
| Placebo | Jardiance | ||
| 10 mg | 25 mg | ||
| N | 225 | 225 | 216 |
| HbA1c (%) | |||
| Valor basal (media) | 8,15 | 8,07 | 8,10 |
| Cambio respecto al valor basal1 | -0,17 | -0,82 | -0,77 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,64* (-0,79, -0,49) | -0,59* (-0,74, -0,44) | |
| N | 216 | 209 | 202 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 %2 | 9,3 | 26,3 | 32,2 |
| N | 225 | 225 | 216 |
| Peso corporal (kg) | |||
| Valor basal (media) | 76,23 | 77,08 | 77,50 |
| Cambio respecto al valor basal1 | -0,39 | -2,16 | -2,39 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -1,76* (-2,25, -1,28) | -1,99* (-2,48, -1,50) | |
| N | 225 | 225 | 216 |
| PAS (mm Hg)2 | |||
| Valor basal (media) | 128,8 | 128,7 | 129,3 |
| Cambio respecto al valor basal1 | -1,4 | -4,1 | -3,5 |
| Diferencia respecto al placebo1 (IC del 95 %) | -2,7 (-4,6, -0,8) | -2,1 (-4,0, -0,2) | |
| Tratamiento con pioglitazona +/- metformina | |||
| Placebo | Jardiance | ||
| 10 mg | 25 mg | ||
| N | 165 | 165 | 168 |
| HbA1c (%) | |||
| Valor basal (media) | 8,16 | 8,07 | 8,06 |
| Cambio respecto al valor basal1 | -0,11 | -0,59 | -0,72 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,48* (-0,69, -0,27) | -0,61* (-0,82, -0,40) | |
| N | 155 | 151 | 160 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 %2 | 7,7 | 24 | 30 |
| N | 165 | 165 | 168 |
| Peso corporal (kg) | |||
| Valor basal (media) | 78,1 | 77,97 | 78,93 |
| Cambio respecto al valor basal1 | 0,34 | -1,62 | -1,47 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -1,95* (-2,64, -1,27) | -1,81* (-2,49, -1,13) | |
| N | 165 | 165 | 168 |
| PAS (mm Hg)3 | |||
| Valor basal (media) | 125,7 | 126,5 | 126 |
| Cambio respecto al valor basal1 | 0,7 | -3,1 | -4,0 |
| Diferencia respecto al placebo1 (IC del 95 %) | -3,9 (-6,23, -1,50) | -4,7 (-7,08, -2,37) | |
a Grupo completo de análisis (FAS) utilizando la última observación considerada (LOCF) antes del
tratamiento de rescate glucémico
1 Media ajustada respecto al valor basal
2 No evaluado en cuanto a significación estadística debido al resultado del procedimiento de prueba confirmatorio secuencial
3 LOCF, valores censurados estadísticamente después del rescate antihipertensivo
* valor p<0,0001
En combinación con metformina en pacientes sin tratamiento previo
Se realizó un estudio de diseño factorial de 24 semanas de duración para evaluar la eficacia y seguridad de empagliflozina en pacientes sin tratamiento previo. El tratamiento con empagliflozina en combinación con metformina (5 mg y 500 mg; 5 mg y 1 000 mg; 12,5 mg y 500 mg; y 12,5 mg y 1 000 mg administrados dos veces al día) proporcionó mejoras estadísticamente significativas en la HbA1c (Tabla 4) y dio lugar a unas reducciones mayores en la GPA (en comparación con los componentes individuales) y en el peso corporal (en comparación con metformina).
Tabla 4: Resultados de eficacia en la semana 24 en los que se compara empagliflozina en combinación con metformina frente a los componentes individualesa
| Empagliflozina 10 mgb | Empagliflozina 25 mgb | Metforminac | |||||||
| +Met 1 000 mgc | +Met 2 000 mgc | Sin Met | +Met 1 000 mgc | +Met 2 000 mgc | Sin Met | 1 000 mg | 2 000 mg | ||
| N | 161 | 167 | 169 | 165 | 169 | 163 | 167 | 162 | |
| HbA1c (%) | |||||||||
| Valor basal (media) | 8,68 | 8,65 | 8,62 | 8,84 | 8,66 | 8,86 | 8,69 | 8,55 | |
| Cambio respecto al valor basal1 | -1,98 | -2,07 | -1,35 | -1,93 | -2,08 | -1,36 | -1,18 | -1,75 | |
| Comparación frente a empa (IC del 95 %)1 | -0,63* (-0,86, -0,40) | -0,72* (-0,96, -0,49) | -0,57* (-0,81, -0,34) | -0,72* (-0,95, -0,48) | |||||
| Comparación frente a met (IC del 95 %)1 | -0,79* (-1,03, -0,56) | -0,33* (-0,56, -0,09) | -0,75* (-0,98, -0,51) | -0,33* (-0,56, -0,10) | |||||
Met = metformina; empa = empagliflozina
1media ajustada respecto al valor basal
aLos análisis se realizaron en el grupo de análisis completo (FAS) utilizando un método de casos observados (CO)
bAdministrada en dos dosis iguales divididas al día cuando se administra con metformina
cAdministrada en dos dosis iguales divididas al día
*p≤0,0062 para HbA1c
Empagliflozina en pacientes no controlados de forma adecuada con metformina y linagliptina
En pacientes no controlados de forma adecuada con metformina y linagliptina 5 mg, el tratamiento con 10 mg y 25 mg de empagliflozina dio lugar a reducciones estadísticamente significativas (p < 0,0001) en la HbA1c y en el peso corporal en comparación con el placebo (Tabla 5). Además, dio lugar a reducciones de importancia clínica en la GPA y en la tensión arterial sistólica y diastólica en comparación con el placebo.
Tabla 5: Resultados de eficacia de un estudio controlado con placebo de 24 semanas en pacientes no controlados de forma adecuada con metformina y linagliptina 5 mg
| Adición a metformina y linagliptina 5 mg | |||
| Placebo5 | Empagliflozina6 | ||
| 10 mg | 25 mg | ||
| N | 106 | 109 | 110 |
| HbA1c (%)3 | |||
| Basal (media) | 7,96 | 7,97 | 7,97 |
| Cambio respecto al valor basal1 | 0,14 | -0,65 | -0,56 |
| Difirencia con el placebo (IC del 95 %) | -0,79* (-1,02, -0,55) | -0,70* (-0,93, -0,46) | |
| N | 100 | 100 | 107 |
| Pacientes (%) que logran una HbA1c <7 % con una HbA1c basal ≥7 %2 | 17,0 | 37,0 | 32,7 |
| N | 106 | 109 | 110 |
| Peso corporal (kg)3 | |||
| Basal (media) | 82,3 | 88,4 | 84,4 |
| Cambio respecto al valor basal1 | -0,3 | -3,1 | -2,5 |
| Difirencia con el placebo (IC del 95 %) | -2,8* (-3,5, -2,1) | -2,2* (-2,9, -1,5) | |
| N | 106 | 109 | 110 |
| TAS (mm Hg)4 | |||
| Basal (media) | 130,1 | 130,4 | 131,0 |
| Cambio respecto al valor basal1 | -1,7 | -3,0 | -4,3 |
| Difirencia con el placebo (IC del 95 %) | -1,3 (-4,2, 1,7) | -2,6 (-5,5, 0,4) | |
1 Media ajustada respecto al valor basal
2 No evaluado con fines de significación estadística; no forma parte del procedimiento de análisis secuencial para las variables secundarias
3 El modelo mixto de medidas repetidas (MMRM) en el FAS (CO [casos observados]) incluyó la HbA1c basal, TFGe basal (modificación de la dieta en el estudio de la enfermedad renal, MDRD), región geográfica, visita, tratamiento y tratamiento por interacción de la visita. Para el peso, se incluyó el basal.
4 El modelo mmRM incluyó la TAS basal y la HbA1c basal como covariable(s) lineal(es), y la TFGe basal, región geográfica, visita, tratamiento y visita por interacción con el tratamiento como efectos fijos.
5 Los pacientes aleatorizados al grupo de placebo recibieron placebo más linagliptina 5 mg con metformina base
6 Los pacientes aleatorizados a los grupos de empagliflozina 10 mg o 25 mg recibieron empagliflozina 10 mg o 25 mg y linagliptina 5 mg con metformina base
* Valor de p<0,0001
En un subgrupo previamente especificado de pacientes con HbA1c basal mayor o igual al 8,5 % la reducción con respecto al valor basal en la HbA1c fue del -1.3 % con empagliflozina 10 mg o 25 mg a las 24 semanas (p<0,0001) en comparación con el placebo.
Datos de empagliflozina de 24 meses, como tratamiento de adición a metformina en comparación con glimepirida
En un ensayo que comparó la eficacia y seguridad de empagliflozina 25 mg frente a glimepirida (hasta 4 mg al día) en pacientes con un control glucémico inadecuado con metformina sola, el tratamiento diario con empagliflozina dio lugar a una mayor reducción de la HbA1c (Tabla 6) y a una reducción clínicamente significativa de la GPA en comparación con glimepirida. La administración diaria de empagliflozina provocó una reducción estadísticamente significativa del peso corporal y de la presión arterial sistólica y diastólica, y una proporción inferior de pacientes estadísticamente significativa con episodios hipoglucémicos en comparación con glimepirida (2,5 % para empagliflozina, 24,2 % para glimepirida, p<0,0001).
Tabla 6: Resultados de eficacia en la semana 104 de un ensayo controlado con activo que comparó empagliflozina con glimepirida en adición a metforminaa
| Empagliflozina 25 mg | Glimepiridab | |
| N | 765 | 780 |
| HbA1c (%) | ||
| Valor basal (media) | 7,92 | 7,92 |
| Cambio respecto al valor basal1 | -0,66 | -0,55 |
| Diferencia respecto a glimepirida1 (IC del 97,5 %) | -0,11* (-0,20, -0,01) | |
| N | 690 | 715 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 %2 | 33,6 | 30,9 |
| N | 765 | 780 |
| Peso corporal (kg) | ||
| Valor basal (media) | 82,52 | 83,03 |
| Cambio respecto al valor basal1 | -3,12 | 1,34 |
| Diferencia respecto a glimepirida1 (IC del 97,5 %) | -4,46** (-4,87, -4,05) | |
| N | 765 | 780 |
| PAS (mm Hg)2 | ||
| Valor basal (media) | 133,4 | 133,5 |
| Cambio respecto al valor basal1 | -3,1 | 2,5 |
| Diferencia respecto a glimepirida1 (IC del 97,5 %) | -5,6** (-7,0, -4,2) | |
a Grupo completo de análisis (FAS) utilizando la última observación considerada (LOCF) antes del tratamiento de rescate glucémico
b Hasta 4 mg de glimepirida
1 Media ajustada respecto al valor basal
2 LOCF, valores censurados estadísticamente después del rescate antihipertensivo
* valor p<0,0001 para no inferioridad, y valor p = 0,0153 para superioridad
** valor p<0,0001
Tratamiento de adición a insulina
Empagliflozina añadida a dosis diarias múltiples de insulina
Se evaluó la eficacia y seguridad de empagliflozina como tratamiento de adición a dosis diarias múltiples de insulina con o sin metformina concomitante en un ensayo doble ciego controlado con placebo de 52 semanas de duración. Durante las 18 primeras semanas y las 12 últimas semanas, la dosis de insulina se mantuvo estable, pero se ajustó entre las semanas 19 y 40 para alcanzar niveles de glucosa preprandial <100 mg/dl [5,5 mmol/l] y niveles de glucosa posprandial <140 mg/dl [7,8 mmol/l].
En la semana 18, empagliflozina presentó una mejora estadísticamente significativa de la HbA1c en comparación con el placebo (Tabla 7).
En la semana 52, el tratamiento con empagliflozina provocó una reducción estadísticamente significativa de la HbA1c y un ahorro de insulina en comparación con el placebo, así como una reducción en la GPA y el peso corporal.
Tabla 7: Resultados de eficacia en las semanas 18 y 52 de un ensayo controlado con placebo de empagliflozina como tratamiento de adición a dosis múltiples diarias de insulina con o sin metformina
| Placebo | Jardiance | ||
| 10 mg | 25 mg | ||
| N | 188 | 186 | 189 |
| HbA1c (%) en la semana 18 | |||
| Valor basal (media) | 8,33 | 8,39 | 8,29 |
| Cambio respecto al valor basal1 | -0,50 | -0,94 | -1,02 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,44* (-0,61, -0,27) | -0,52* (-0,69, -0,35) | |
| N | 115 | 119 | 118 |
| HbA1c (%) en la semana 522 | |||
| Valor basal (media) | 8,25 | 8,40 | 8,37 |
| Cambio respecto al valor basal1 | -0,81 | -1,18 | -1,27 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,38*** (-0,62, -0,13) | -0,46* (-0,70, -0,22) | |
| N | 113 | 118 | 118 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 % en la semana 52 | 26,5 | 39,8 | 45,8 |
| N | 115 | 118 | 117 |
| Valor basal (media) | 89,94 | 88,57 | 90,38 |
| Cambio respecto al valor basal1 | 10,16 | 1,33 | -1,06 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -8,83# (-15,69, -1,97) | -11,22** (-18,09, -4,36) | |
| N | 115 | 119 | 118 |
| Valor basal (media) | 96,34 | 96,47 | 95,37 |
| Cambio respecto al valor basal1 | 0,44 | -1,95 | -2,04 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -2,39* (-3,54, -1,24) | -2,48* (-3,63, -1,33) | |
1 Media ajustada respecto al valor basal
2 Semana 19-40: pauta de tratamiento hasta alcanzar el objetivo con ajuste de la dosis de insulina para conseguir niveles objetivo de glucosa predefinidos (preprandial <100 mg/dl (5,5 mmol/l), posprandial <140 mg/dl (7,8 mmol/l)
* valor p<0,0001
** valor p = 0,0003
*** valor p = 0,0005
# valor p = 0,0040
Empagliflozina como tratamiento de adición a insulina basal
Se evaluó la eficacia y seguridad de empagliflozina como tratamiento de adición a insulina basal con o sin metformina y/o una sulfonilurea en un ensayo doble ciego controlado con placebo de 78 semanas de duración. Durante las 18 primeras semanas, la dosis de insulina se mantuvo estable, pero se ajustó para lograr una GPA <110 mg/dl en las 60 semanas siguientes.
En la semana 18, empagliflozina presentó una mejora estadísticamente significativa en la HbA1c (Tabla 8).
En la semana 78, empagliflozina provocó una disminución estadísticamente significativa de la HbA1c y un ahorro de insulina en comparación con placebo. Además, empagliflozina dio lugar a una reducción de la GPA, el peso corporal y la presión arterial.
Tabla 8: Resultados de eficacia en las semanas 18 y 78 de un ensayo controlado con placebo de empagliflozina como tratamiento de adición a insulina basal con o sin metformina o una sulfonilureaa
| Placebo | Empagliflozina 10 mg | Empagliflozina 25 mg | |
| N | 125 | 132 | 117 |
| HbA1c (%) en la semana 18 | |||
| Valor basal (media) | 8,10 | 8,26 | 8,34 |
| Cambio respecto al valor basal1 | -0,01 | -0,57 | -0,71 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,56* (-0,78, -0,33) | -0,70* (-0,93, -0,47) | |
| N | 112 | 127 | 110 |
| HbA1c (%) en la semana 78 | |||
| Valor basal (media) | 8,09 | 8,27 | 8,29 |
| Cambio respecto al valor basal1 | -0,02 | -0,48 | -0,64 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -0,46* (-0,73, -0,19) | -0,62* (-0,90, -0,34) | |
| N | 112 | 127 | 110 |
| Dosis de insulina basal (UI/día) en la semana 78 | |||
| Valor basal (media) | 47,84 | 45,13 | 48,43 |
| Cambio respecto al valor basal1 | 5,45 | -1,21 | -0,47 |
| Diferencia respecto al placebo1 (IC del 97,5 %) | -6,66** (-11,56, -1,77) | -5,92** (-11,00, -0,85) |
a Grupo completo de análisis (FAS): pacientes que completaron el estudio utilizando la última observación considerada (LOCF) antes del tratamiento de rescate glucémico
1 Media ajustada respecto al valor basal
* valor p<0,0001
** valor p<0,025
Pacientes con insuficiencia renal, datos controlados con placebo de 52 semanas
Se evaluó la eficacia y seguridad de empagliflozina como tratamiento de adición a un tratamiento antidiabético en pacientes con insuficiencia renal en un estudio doble ciego controlado con placebo de 52 semanas de duración. En la semana 24, el tratamiento con empagliflozina provocó una reducción estadísticamente significativa de la HbA1c (Tabla 9) y una mejora clínicamente significativa en la GPA en comparación con placebo. La mejora en la HbA1c, el peso corporal y la presión arterial se mantuvo durante 52 semanas.
Tabla 9: Resultados en la semana 24 de un estudio controlado con placebo de empagliflozina en pacientes con diabetes tipo 2 e insuficiencia renala
| Placebo | Empagliflozina 10 mg | Empagliflozin a 25 mg | Placebo | Empagliflozin a 25 mg | |
| TFGe ≥60 a <90 ml/min/1,73 m2 | TFGe ≥30 a <60 ml/min/1,73 m2 | ||||
| N | 95 | 98 | 97 | 187 | 187 |
| HbA1c (%) | |||||
| Valor basal (media) | 8,09 | 8,02 | 7,96 | 8,04 | 8,03 |
| Cambio respecto al valor basal1 | 0,06 | -0,46 | -0,63 | 0,05 | -0,37 |
| Diferencia respecto al placebo1 (IC del 95 %) | -0,52* (-0,72, -0,32) | -0,68* (-0,88, -0,49) | -0,42* (-0,56, -0,28) | ||
| N | 89 | 94 | 91 | 178 | 175 |
| Pacientes (%) que logran un valor de HbA1c <7 % con un valor basal de la HbA1c ≥7 %2 | 6,7 | 17,0 | 24,2 | 7,9 | 12,0 |
| N | 95 | 98 | 97 | 187 | 187 |
| Peso corporal (kg)2 | |||||
| Valor basal (media) | 86,00 | 92,05 | 88,06 | 82,49 | 83,22 |
| Cambio respecto al valor basal1 | -0,33 | -1,76 | -2,33 | -0,08 | -0,98 |
| Diferencia respecto al placebo1 (IC del 95 %) | -1,43 (-2,09, -0,77) | -2,00 (-2,66, -1,34) | -0,91 (-1,41, -0,41) | ||
| N | 95 | 98 | 97 | 187 | 187 |
| PAS (mm Hg)2 | |||||
| Valor basal (media) | 134,69 | 137,37 | 133,68 | 136,38 | 136,64 |
| Cambio respecto al valor basal1 | 0,65 | -2,92 | -4,47 | 0,40 | -3,88 |
| Diferencia respecto al placebo1 (IC del 95 %) | -3,57 (-6,86, -0,29) | -5,12 (-8,41, -1,82) | -4,28 (-6,88, -1,68) | ||
a Grupo completo de análisis (FAS) utilizando la última observación considerada (LOCF) antes del tratamiento de rescate glucémico
1 Media ajustada respecto al valor basal
2 No evaluado en cuanto a significación estadística debido al resultado del procedimiento de prueba confirmatorio secuencial
* p<0,0001
Resultados cardiovasculares
El ensayo doble ciego controlado con placebo EMPA-REG OUTCOME comparó dosis agrupadas de empagliflozina 10 mg y 25 mg con placebo asociadas al tratamiento de referencia en pacientes con diabetes tipo 2 y enfermedad cardiovascular establecida. Se trató a un total de 7 020 pacientes (empagliflozina 10 mg: 2 345, empagliflozina 25 mg: 2 342, placebo: 2 333) y se les realizó seguimiento durante una media de 3,1 años. La edad media fue de 63 años, la media de la HbA1c fue del 8,1 %, y el 71,5 % eran varones. Al inicio, el 74 % de los pacientes se estaban tratando con metformina, el 48 % con insulina y el 43 % con una sulfonilurea. Alrededor de la mitad de los pacientes (52,2 %) tenían una TFGe de 60-90 ml/min/1,73 m2, el 17,8 % de 45-60 ml/min/1,73 m2 y el 7,7 % de 30-45 ml/min/1,73 m2.
En la semana 12 se observó una mejora de la media ajustada (DE) en la HbA1c, cuando se comparó con el valor basal, del 0,11 % (0,02) en el grupo de placebo, y del 0,65 % (0,02) y 0,71 % (0,02) en los grupos de empagliflozina 10 y 25 mg. Tras las primeras 12 semanas, el control glucémico se optimizó de manera independiente del tratamiento en investigación. Por tanto, el efecto se atenuó en la semana 94, con una mejora de la media ajustada (DE) en la HbA1c del 0,08 % (0,02) en el grupo de placebo, y del 0,50 % (0,02) y 0,55 % (0,02) en los grupos de empaglflozina 10 y 25 mg.
Empagliflozina fue superior en prevenir la variable primaria compuesta de muerte cardiovascular, infarto de miocardio no mortal o accidente cerebrovascular no mortal comparado con placebo. El efecto del tratamiento se observó mediante una reducción significativa en la muerte cardiovascular sin cambio significativo en el infarto de miocardio no mortal o en el accidente cerebrovascular no mortal.
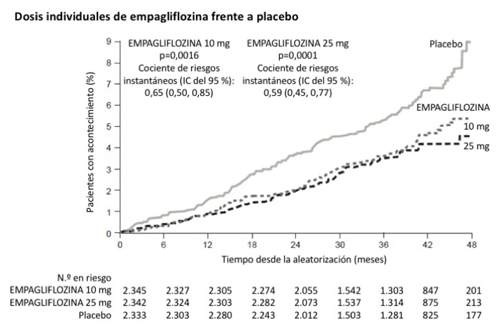
La reducción de la muerte cardiovascular fue comparable para empagliflozina 10 mg y 25 mg (Figura 1) y confirmada mediante una mejora de la supervivencia global (Tabla 10). El efecto de empagliflozina sobre la variable primaria compuesta de muerte cardiovascular, infarto de miocardio no mortal o accidente cerebrovascular no mortal fue en gran medida independiente del control glucémico o de la función renal (TFGe) y, en general, similar en las distintas categorías de TFGe hasta una TFGe de 30 ml/min/1,73 m2 en el estudio EMPA-REG OUTCOME.
La eficacia en la prevención de la mortalidad cardiovascular no se ha establecido de manera concluyente en pacientes tratados con empagliflozina de forma concomitante con inhibidores de la DPP-4 o en pacientes de raza negra debido a que la representación de estos grupos en el estudio EMPA-REG OUTCOME fue limitada.
Tabla 10: Efecto del tratamiento para la variable primaria compuesta, sus componentes y mortalidada
| Placebo | Empagliflozinab | |
| N | 2 333 | 4 687 |
| Tiempo hasta el primer acontecimiento de muerte CV, IM no mortal o accidente cerebrovascular no mortal) N (%) | 282 (12,1) | 490 (10,5) |
| Cociente de riesgo intantáneo (Hazard ratio) frente a placebo (IC del 95,02 %)* | 0,86 (0,74, 0,99) | |
| Valor p para la superioridad | 0,0382 | |
| Muerte CV N (%) | 137 (5,9) | 172 (3,7) |
| Cociente de riesgo intantáneo (Hazard ratio) frente a placebo (IC del 95 %) | 0,62 (0,49, 0,77) | |
| Valor p | <0,0001 | |
| IM no mortal N (%) | 121 (5,2) | 213 (4,5) |
| Cociente de riesgo intantáneo (Hazard ratio) frente a placebo (IC del 95 %) | 0,87 (0,70, 1,09) | |
| Valor p | 0,2189 | |
| Accidente cerebrovascular no mortal N (%) | 60 (2,6) | 150 (3,2) |
| Cociente de riesgo intantáneo (Hazard ratio) frente a placebo (IC del 95 %) | 1,24 (0,92, 1,67) | |
| Valor p | 0,1638 | |
| Mortalidad por todas las causas N (%) | 194 (8,3) | 269 (5,7) |
| Cociente de riesgo intantáneo (Hazard ratio) frente a placebo (IC del 95 %) | 0,68 (0,57, 0,82) | |
| Valor p | <0,0001 | |
| Mortalidad no CV N (%) | 57 (2,4) | 97 (2,1) |
| Cociente de riesgo intantáneo (Hazard ratio) frente a placebo (IC del 95 %) | 0,84 (0,60, 1,16) |
CV = cardiovascular, IM = infarto de miocardio
a Conjunto tratado (CT), es decir, pacientes que han recibido al menos una dosis del medicamento del estudio
b Dosis agrupadas de empagliflozina 10 mg y 25 mg
* Puesto que los datos del ensayo se incluyeron en un análisis provisional, se aplica un intervalo de confianza bilateral del 95,02 % que corresponde a un valor p menor de 0,0498 para la significación.
Figura 1: Tiempo hasta la aparición de muerte cardiovascular en el ensayo EMPA-REG OUTCOME
Insuficiencia cardíaca que requiere hospitalización
En el ensayo EMPA-REG OUTCOME, empagliflozina redujo el riesgo de hospitalización por insuficiencia cardíaca en comparación con el placebo (empagliflozina 2,7 %; placebo 4,1 %. Cociente de riesgos instantáneos [Hazard ratio, HR] 0,65, IC del 95 % 0,50, 0,85).
Nefropatía
En el ensayo EMPA-REG OUTCOME, en relación al tiempo hasta el primer acontecimiento de nefropatía, la HR fue de 0,61 (IC del 95 % 0,53, 0,70) para empagliflozina (12,7 %) en comparación con el placebo (18,8 %).
Además, empagliflozina mostró una incidencia mayor (HR 1,82, IC del 95 % 1,40, 2,37) de normoalbuminuria o microalbuminuria sostenida (49,7 %) en los pacientes con macroalbuminuria basal en comparación con el placebo (28,8 %).
Glucosa plasmática en ayunas
En cuatro ensayos controlados con placebo, el tratamiento con empagliflozina en monoterapia o como tratamiento de adición a metformina, pioglitazona o metformina más una sulfonilurea provocó cambios medios respecto al valor basal de GPA de -20,5 mg/dl [-1,14 mmol/l] para empagliflozina 10 mg y de -23,2 mg/dl [-1,29 mmol/l] para empagliflozina 25 mg en comparación con el placebo (7,4 mg/dl [0,41 mmol/l]). Este efecto se observó después de 24 semanas y se mantuvo durante 76 semanas.
Glucosa posprandial a las 2 horas
El tratamiento con empagliflozina como adición a metformina o metformina y una sulfonilurea provocó una reducción clínicamente significativa de la glucosa posprandial a las 2 horas (prueba de tolerancia a la glucosa) a las 24 semanas (tratamiento de adición a metformina: placebo +5,9 mg/dl, empagliflozina 10 mg: -46,0 mg/dl, empagliflozina 25 mg: -44,6 mg/dl, tratamiento de adición a metformina y una sulfonilurea: placebo -2,3 mg/dl, empagliflozina 10 mg: -35,7 mg/dl, empagliflozina 25 mg: -36,6 mg/dl).
Pacientes con un valor basal alto de la HbA1c >10 %
En un análisis conjunto pre-especificado de tres estudios de fase 3, el tratamiento abierto con empagliflozina 25 mg en pacientes con hiperglucemia grave (N = 184, valor basal medio de HbA1c 11,15 %) provocó una reducción clínicamente significativa en la HbA1c respecto al valor basal del 3,27 % en la semana 24; en estos estudios no se incluyó ningún grupo de placebo ni de empagliflozina 10 mg.
Peso corporal
En un análisis conjunto pre-especificado de 4 estudios controlados con placebo, el tratamiento con empagliflozina provocó una reducción del peso corporal (-0,24 kg para placebo, -2,04 kg para empagliflozina 10 mg y -2,26 kg para empagliflozina 25 mg) en la semana 24, que se mantuvo hasta la semana 52 (-0,16 kg para placebo, -1,96 kg para empagliflozina 10 mg y -2,25 kg para empagliflozina 25 mg).
Presión arterial
La eficacia y seguridad de empagliflozina se evaluó en un ensayo doble ciego controlado con placebo de 12 semanas de duración, en pacientes con diabetes tipo 2 y presión arterial alta que seguían diferentes tratamientos antidiabéticos y hasta 2 tratamientos antihipertensivos. El tratamiento con empagliflozina una vez al día provocó una mejora estadísticamente significativa en la HbA1c, y en la presión arterial sistólica y diastólica media de 24 horas, determinada mediante controles ambulatorios de la presión arterial (Tabla 11). El tratamiento con empagliflozina provocó reducciones en la PAS y PAD en posición sentada.
Tabla 11: Resultados de eficacia en la semana 12 de un ensayo controlado con placebo de empagliflozina en pacientes con diabetes tipo 2 y presión arterial no controladaa
| Placebo | Jardiance | ||
| 10 mg | 25 mg | ||
| N | 271 | 276 | 276 |
| HbA1c (%) en la semana 121 | |||
| Valor basal (media) | 7,90 | 7,87 | 7,92 |
| Cambio respecto al valor basal2 | 0,03 | -0,59 | -0,62 |
| Diferencia respecto al placebo2 (IC del 95 %) | -0,62* (-0,72, -0,52) | -0,65* (-0,75, -0,55) | |
| PAS a las 24 horas en la semana 123 | |||
| Valor basal (media) | 131,72 | 131,34 | 131,18 |
| Cambio respecto al valor basal4 | 0,48 | -2,95 | -3,68 |
| Diferencia respecto al placebo4 (IC del 95 %) | -3,44* (-4,78, -2,09) | -4,16* (-5,50, -2,83) | |
| PAD a las 24 horas en la semana 123 | |||
| Valor basal (media) | 75,16 | 75,13 | 74,64 |
| Cambio respecto al valor basal5 | 0,32 | -1,04 | -1,40 |
| Diferencia respecto al placebo5 (IC del 95 %) | -1,36** (-2,15, -0,56) | -1,72* (-2,51, -0,93) | |
a Grupo completo de análisis (FAS)
1 LOCF, valores censurados estadísticamente después del tratamiento de rescate antidiabético
2 Media ajustada respecto a la HbA1c basal, la TFGe basal, la región geográfica y el número de medicamentos antihipertensivos
3 LOCF, valores censurados estadísticamente después del tratamiento de rescate antidiabético o de cambiar el tratamiento de rescate antihipertensivo
4 Media ajustada respecto a la PAS basal la HbA1c basal, la TFGe basal, la región geográfica y el número de medicamentos antihipertensivos
5 Media ajustada respecto a la PAD basal, la HbA1c basal, la TFGe basal, la región geográfica y el número de medicamentos antihipertensivos
* valor p<0,0001
** valor p<0,001
En un análisis conjunto pre-especificado de 4 estudios controlados con placebo, el tratamiento con empagliflozina provocó una reducción de la presión arterial sistólica (empagliflozina 10 mg: -3,9 mm Hg; empagliflozina 25 mg: -4,3 mm Hg) en comparación con placebo (-0,5 mm Hg) y de la presión arterial diastólica (empagliflozina 10 mg: -1,8 mm Hg; empagliflozina 25 mg: -2,0 mm Hg) en comparación con placebo (-0,5 mm Hg) en la semana 24 y esta reducción se mantuvo hasta la semana 52.
Insuficiencia cardíaca
Empagliflozina en pacientes con insuficiencia cardíaca y fracción de eyección reducida
Se realizó un estudio aleatorizado, doble ciego y controlado con placebo (EMPEROR-Reduced) en 3 730 pacientes con insuficiencia cardíaca crónica (clases II-IV de la New York Heart Association [NYHA]) y fracción de eyección reducida (FEVI ≤40 %) para evaluar la eficacia y la seguridad de empagliflozina en dosis de 10 mg una vez al día como adyuvante del tratamiento convencional de la insuficiencia cardíaca. La variable primaria fue el tiempo hasta el primer acontecimiento adjudicado de muerte por causas cardiovasculares (CV) u hospitalización por insuficiencia cardíaca (HIC). La aparición de HIC adjudicada (primera y recurrente) y la pendiente del cambio de la TFGe (CKD-EPI)cr con respecto al valor inicial se incluyeron en el análisis de confirmación. El tratamiento de la insuficiencia cardíaca en el momento inicial incluyó inhibidores de la ECA/antagonistas de los receptores de la angiotensina/inhibidores de los receptores de la angiotensina y de la neprilisina (88,3 %), betabloqueantes (94,7 %), antagonistas de los receptores de mineralocorticoides (71,3 %) y diuréticos (95,0 %).
Un total de 1 863 pacientes fueron asignados aleatoriamente para recibir empagliflozina en dosis de 10 mg (placebo: 1 867) con un seguimiento durante una mediana de 15,7 meses. La población del estudio estaba formada por un 76,1 % de hombres y un 23,9 % de mujeres con una media de edad de 66,8 años (intervalo: 25-94 años), el 26,8 % tenía 75 años de edad o más, el 70,5 % de la población del estudio era de raza blanca, el 18,0 % eran asiáticos y el 6,9 % eran afroamericanos. En el momento de la aleatorización, el 75,1 % de los pacientes estaba en la clase II de la NYHA, el 24,4 % estaba en la clase III y el 0,5 % estaba en la clase IV. La FEVI media era del 27,5 %. En el momento inicial, la TFGe media era de 62,0 ml/min/1,73 m2 y la mediana del cociente albúmina-creatinina en orina (CACO) era de 22 mg/g. Aproximadamente la mitad de los pacientes (51,7 %) tenía una TFGe ≥60 ml/min/1,73 m2, el 24,1 % tenía una TFGe de entre 45 y 60 ml/min/1,73 m2, el 18,6 % tenía una TFGe de entre 30 y 45 ml/min/1,73 m2 y el 5,3 % tenía una TFGe de entre 20 y 30 ml/min/1,73 m2.
Empagliflozina fue superior en la reducción del riesgo de la variable primaria compuesta de muerte por causas cardiovasculares u hospitalización por insuficiencia cardíaca en comparación con el placebo. Además, empagliflozina redujo significativamente el riesgo de HIC (primera y recurrente) y redujo significativamente la tasa de descenso de la TFGe (Tabla 12; Figura 2).
Tabla 12: Efecto del tratamiento para la variable primaria compuesta, sus componentes y las dos variables secundarias claves en el análisis de confirmación previamente especificado
| Placebo | Empagliflozina 10 mg | |
| N | 1 867 | 1 863 |
| Tiempo hasta el primer acontecimiento de muerte por causas CV o HIC, N (%) | 462 (24,7) | 361 (19,4) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %)* | 0,75 (0,65, 0,86) | |
| Valor de p para la superioridad | <0,0001 | |
| Muerte por causas CV, N (%) | 202 (10,8) | 187 (10,0) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,92 (0,75, 1,12) | |
| HIC (primera), N (%) | 342 (18,3) | 246 (13,2) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,69 (0,59, 0,81) | |
| HIC (primera y recurrente), N de acontecimientos | 553 | 388 |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %)* | 0,70 (0,58, 0,85) | |
| Valor de p | 0,0003 | |
| Pendiente de la TFGe (CKD-EPI)cr**, tasa de descenso (ml/min/1,73 m2/año) | –2,28 | –0,55 |
| Diferencia del tratamiento frente al placebo (IC del 95 %) | 1,73 (1,10, 2,37) | |
| Valor de p | <0,0001 |
CV = cardiovascular; HIC = hospitalización por insuficiencia cardíaca; TFGe = tasa de filtración glomerular estimada; CKD EPI = ecuación del grupo Chronic Kidney Disease Epidemiology Collaboration
* Los acontecimientos de muerte por causas CV y HIC fueron adjudicados por un comité de acontecimientos clínicos independiente y analizados en el conjunto de pacientes aleatorizados.
**La pendiente de la TFGe se analizó en el conjunto de pacientes tratados. La ordenada en el origen es –0,95 ml/min/1,73 m2 para el placebo y –3,02 ml/min/1,73 m2 para empagliflozina. La ordenada en el origen representa el efecto agudo sobre la TFGe, mientras que la pendiente representa el efecto a largo plazo.
Figura 2 Tiempo hasta el primer acontecimiento adjudicado de muerte por causas CV o HIC

Los resultados de la variable primaria compuesta fueron generalmente homogéneos, con un cociente de riesgos instantáneos (HR) inferior a 1 en los subgrupos previamente especificados, incluidos los pacientes con insuficiencia cardíaca, con o sin diabetes tipo 2 y con o sin insuficiencia renal (hasta una TFGe de 20 ml/min/1,73 m2).
Empagliflozina en pacientes con insuficiencia cardíaca y fracción de eyección preservada
Se realizó un estudio aleatorizado, doble ciego y controlado con placebo (EMPEROR-Preserved) en 5 988 pacientes con insuficiencia cardíaca crónica (clases II-IV de la NYHA) y fracción de eyección preservada (FEVI >40 %) para evaluar la eficacia y la seguridad de empagliflozina en dosis de 10 mg una vez al día como adyuvante del tratamiento convencional. La variable primaria fue el tiempo hasta el primer acontecimiento adjudicado de muerte por causas cardiovasculares (CV) u hospitalización por insuficiencia cardíaca (HIC). La aparición de HIC adjudicada (primera y recurrente) y la pendiente del cambio de la TFGe (CKD-EPI)cr con respecto al valor inicial se incluyeron en el análisis de confirmación. El tratamiento inicial incluyó inhibidores de la ECA/antagonistas de los receptores de la angiotensina/inhibidores de los receptores de la angiotensina y de la neprilisina (80,7 %), betabloqueantes (86,3 %), antagonistas de los receptores de mineralocorticoides (37,5 %) y diuréticos (86,2 %).
Un total de 2 997 pacientes fueron asignados aleatoriamente para recibir empagliflozina en dosis de 10 mg (placebo: 2 991) con un seguimiento durante una mediana de 26,2 meses. La población del estudio estaba formada por un 55,3 % de hombres y un 44,7 % de mujeres con una media de edad de 71,9 años (intervalo: 22-100 años), el 43,0 % tenía 75 años de edad o más, el 75,9 % de la población del estudio era de raza blanca, el 13,8 % eran asiáticos y el 4,3 % eran afroamericanos. En el momento de la aleatorización, el 81,5 % de los pacientes estaba en la clase II de la NYHA, el 18,1 % estaba en la clase III y el 0,3 % estaba en la clase IV. La población del estudio EMPEROR-Preserved incluía a pacientes con una FEVI <50 % (33,1 %), con una FEVI entre 50 y <60 % (34,4 %) y con una FEVI ≥60 % (32,5 %). En el momento inicial, la TFGe media era de 60,6 ml/min/1,73 m2 y la mediana del cociente albúmina-creatinina en orina (CACO) era de 21 mg/g. Aproximadamente la mitad de los pacientes (50,1 %) tenía una TFGe ≥60 ml/min/1,73 m2, el 26,1 % tenía una TFGe de entre 45 y 60 ml/min/1,73 m2, el 18,6 % tenía una TFGe de entre 30 y 45 ml/min/1,73 m2 y el 4,9 % tenía una TFGe de entre 20 y 30 ml/min/1,73 m2.
Empagliflozina fue superior en la reducción del riesgo de la variable primaria compuesta de muerte por causas cardiovasculares u hospitalización por insuficiencia cardíaca en comparación con el placebo. Además, empagliflozina redujo significativamente el riesgo de HIC (primera y recurrente) y redujo significativamente la tasa de descenso de la TFGe (Tabla 13; Figura 3).
Tabla 13: Efecto del tratamiento para la variable primaria compuesta, sus componentes y las dos variables secundarias claves en el análisis de confirmación previamente especificado
| Placebo | Empagliflozina 10 mg | |
| N | 2 991 | 2 997 |
| Tiempo hasta el primer acontecimiento de muerte por causas CV o HIC, N (%) | 511 (17,1) | 415 (13,8) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %)* | 0,79 (0,69, 0,90) | |
| Valor de p para la superioridad | 0,0003 | |
| Muerte por causas CV, N (%) | 244 (8,2) | 219 (7,3) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,91 (0,76, 1,09) | |
| HIC (primera), N (%) | 352 (11,8) | 259 (8,6) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,71 (0,60, 0,83) | |
| HIC (primera y recurrente), N de acontecimientos | 541 | 407 |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %)* | 0,73 (0,61, 0,88) | |
| Valor de p | 0,0009 | |
| Pendiente de la TFGe (CKD-EPI)cr**, tasa de descenso (ml/min/1,73 m2/año) | –2,62 | –1,25 |
| Diferencia del tratamiento frente al placebo (IC del 95 %) | 1,36 (1,06, 1,66) | |
| Valor de p | <0,0001 |
CV = cardiovascular; HIC = hospitalización por insuficiencia cardíaca; TFGe = tasa de filtración glomerular estimada; CKD EPI = ecuación del grupo Chronic Kidney Disease Epidemiology Collaboration
* Los acontecimientos de muerte por causas CV y HIC fueron adjudicados por un comité de acontecimientos clínicos independiente y analizados en el conjunto de pacientes aleatorizados.
**La pendiente de la TFGe se analizó en el conjunto de pacientes tratados. La ordenada en el origen es –0,18 ml/min/1,73 m2 para el placebo y –3,02 ml/min/1,73 m2 para empagliflozina. La ordenada en el origen representa el efecto agudo sobre la TFGe, mientras que la pendiente representa el efecto a largo plazo.
Figura 3 Tiempo hasta el primer acontecimiento adjudicado de muerte por causas CV o HIC
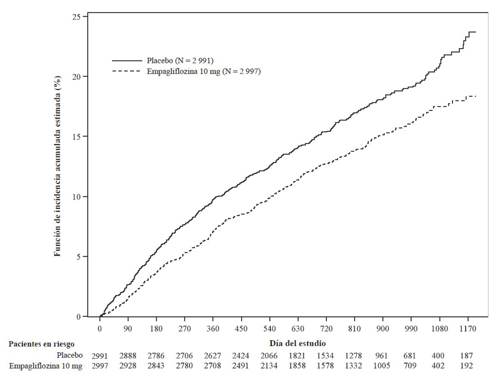
Los resultados de la variable primaria compuesta fueron homogéneos en cada uno de los subgrupos previamente especificados, clasificados en función de, por ejemplo, la FEVI, la presencia o no de diabetes o la función renal (hasta una TFGe de 20 ml/min/1,73 m2).
Enfermedad renal crónica
Se realizó un estudio aleatorizado, doble ciego y controlado con placebo de empagliflozina 10 mg una vez al día (EMPA-KIDNEY) en 6 609 pacientes con enfermedad renal crónica (TFGe entre ≥ 20 y < 45 ml/min/1,73 m2; o TFGe entre ≥ 45 y < 90 ml/min/1,73 m2 con un cociente albúmina-creatinina en orina [CACO] ≥ 200 mg/g) para evaluar variables cardiorrenales como adyuvante del tratamiento convencional. La variable primaria fue el tiempo hasta el primer acontecimiento de progresión de la enfermedad renal (descenso sostenido de la TFGe ≥ 40 % desde la aleatorización, TFGe sostenida < 10 ml/min/1,73 m2, enfermedad renal terminal o muerte por causas renales) o muerte por causas cardiovasculares. En el ensayo de confirmación se incluyó el primer acontecimiento de hospitalización por insuficiencia cardíaca o la muerte por causas cardiovasculares, la hospitalización por cualquier causa (primera y recurrente) y la mortalidad por cualquier causa. El tratamiento de base incluía un uso adecuado de un inhibidor del sistema renina-angiotensina (SRA) (un inhibidor de la enzima convertidora de angiotensina o un antagonista de los receptores de angiotensina en el 85,2 % de los casos).
Se asignó aleatoriamente a un total de 3 304 pacientes a empagliflozina 10 mg (3 305 al placebo), a los que se realizó un seguimiento de una mediana de 24,3 meses. La población del estudio estaba formada por un 66,8 % de hombres y un 33,2 % de mujeres, con una media de edad de 63,3 años (intervalo 18-94 años), y el 23,0 % tenía 75 años de edad o más. El 58,4 % de la población del estudio era de raza blanca, el 36,2 % era de raza asiática y el 4,0 % era de raza negra/afroamericana.
Al inicio del estudio, la TFGe media era de 37,3 ml/min/1,73 m2, el 21,2 % de los pacientes tenía una TFGe ≥ 45 ml/min/1,73 m2, el 44,3 % tenía una TFGe de entre 30 y < 45 ml/min/1,73 m2 y el 34,5 % tenía una TFGe < 30 ml/min/1,73 m2, incluidos 254 pacientes con una TFGe < 20 ml/min/1,73 m2. La mediana del CACO era de 329 mg/g, el 20,1 % de los pacientes tenía un CACO < 30 mg/g, el 28,2 % tenía un CACO de entre 30 y ≤ 300 mg/g y el 51,7 % tenía un CACO > 300 mg/g; el 41,1 % de los pacientes tenía un CACO < 200 mg/g. Las causas primarias de enfermedad renal crónica eran nefropatía diabética/enfermedad renal diabética (31 %), enfermedad glomerular (25 %), enfermedad hipertensiva/renovascular (22 %) y otra/desconocida (22 %).
Empagliflozina fue superior al placebo en la reducción del riesgo de la variable primaria compuesta de progresión de la enfermedad renal o muerte por causas cardiovasculares (ver Tabla 14). Además, empagliflozina redujo significativamente el riesgo de hospitalización por cualquier causa (primera y recurrente).
Tabla 14: Efecto del tratamiento para la variable primaria compuesta, sus componentes y las variables secundarias claves en el análisis de confirmación previamente especificado
| Placebo | Empagliflozina 10 mg | |
| N | 3 305 | 3 304 |
| Tiempo hasta el primer acontecimiento de progresión de la enfermedad renal (descenso sostenido de la TFGe ≥ 40 % desde la aleatorización, TFGe sostenida < 10 ml/min/1,73 m2, enfermedad renal terminal* [ERT] o muerte por causas renales) o muerte por causas CV, N (%) | 558 (16,9) | 432 (13,1) |
| Cociente de riesgos instantáneos frente al placebo (IC del 99,83 %) | 0,72 (0,59, 0,89) | |
| Valor de p para la superioridad | <0,0001 | |
| Descenso sostenido de la TFGe ≥ 40 % desde la aleatorización, N (%) | 474 (14,3) | 359 (10,9) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,70 (0,61, 0,81) | |
| Valor de p | <0,0001 | |
| ERT*o TFGe sostenida < 10 ml/min/1,73 m2, N (%) | 221 (6,7) | 157 (4,8) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,69 (0,56, 0,84) | |
| Valor de p | 0,0003 | |
| Muerte por causas renales, N (%)** | 4 (0,1) | 4 (0,1) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | ||
| Valor de p | ||
| Muerte por causas CV, N (%) | 69 (2,1) | 59 (1,8) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,84 (0,60, 1,19) | |
| Valor de p | 0,3366 | |
| ERT o muerte por causas CV, N (%)# | 217 (6,6) | 163 (4,9) |
| Cociente de riesgos instantáneos frente al placebo (IC del 95 %) | 0,73 (0,59, 0,89) | |
| Valor de p | 0,0023 | |
| Hospitalización por cualquier causa (primera y recurrente), N de acontecimientos | 1 895 | 1 611 |
| Cociente de riesgos instantáneos frente al placebo (IC del 99,03 %) | 0,86 (0,75, 0,98) | |
| Valor de p | 0,0025 |
CV = cardiovascular(es); HIC = hospitalización por insuficiencia cardíaca; TFGe = tasa de filtración glomerular estimada
* La enfermedad renal terminal (ERT) se define como el inicio de la diálisis de mantenimiento o la recepción de un trasplante de riñón.
** Había un número demasiado bajo de acontecimientos de muerte por causas renales para calcular un cociente de riesgos instantáneos fiable.
# Predefinido como uno de los dos criterios de detención en el análisis intermedio previamente planificado.
Figura 4 Tiempo hasta el primer acontecimiento de progresión de la enfermedad renal o hasta el primer acontecimiento adjudicado de muerte por causas CV, función de incidencia acumulada estimada
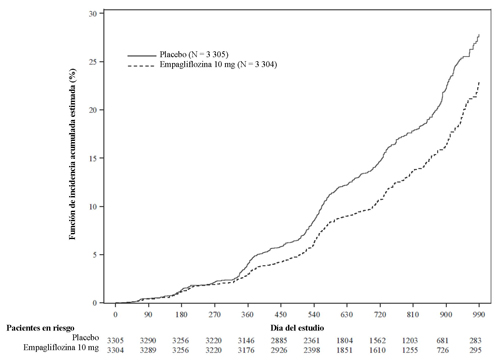
Los resultados de la variable primaria compuesta fueron generalmente homogéneos en los subgrupos previamente especificados, incluidas las categorías de TFGe, la causa subyacente de enfermedad renal, la presencia o ausencia de diabetes o el uso de base de inhibidores del SRA. Los beneficios del tratamiento fueron evidentes de forma más clara en los pacientes con niveles más altos de albuminuria.
Durante el tratamiento, el descenso de la TFGe a lo largo del tiempo fue menor en el grupo de empagliflozina que en el grupo del placebo (Figura 5). Empagliflozina ralentizó la tasa de descenso anual de la TFGe en comparación con el placebo en 1,37 ml/min/1,73 m2/año (IC del 95 % 1,16, 1,59), según un análisis previamente especificado de todas las mediciones de la TFGe obtenidas desde la visita a los 2 meses hasta la visita de seguimiento final. Los pacientes tratados con empagliflozina experimentaron un descenso inicial de la TFGe que retornó hacia el valor basal tras la interrupción del tratamiento tal como muestran varios estudios de empagliflozina, lo cual sugiere que los cambios hemodinámicos intervienen en los efectos agudos de empagliflozina sobre la TFGe.
Figura 5 Cambio en la TFGe a lo largo del tiempo*
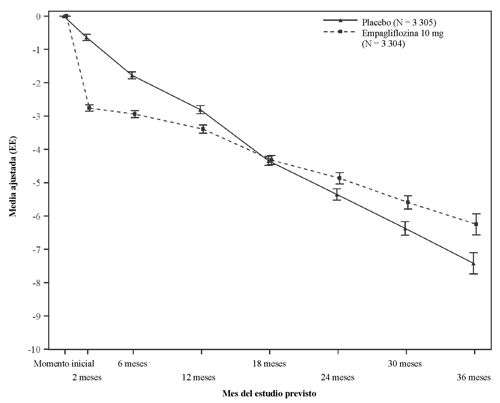
* Resultados de TFGe (CKD-EPI) (ml/min/1,73 m2) de un mmRM a lo largo del tiempo: conjunto de pacientes aleatorizados.
Población pediátrica
Diabetes mellitus tipo 2
Se ha evaluado la eficacia clínica y la seguridad de empagliflozina (10 mg con un posible aumento de dosis a 25 mg) y de linagliptina (5 mg) una vez al día en niños y adolescentes de 10 a 17 años de edad con diabetes mellitus tipo 2 en un estudio controlado con placebo (DINAMO) durante 26 semanas, con un periodo de extensión de seguridad de hasta 52 semanas. Entre los tratamientos de base como complemento a la dieta y el ejercicio se incluyeron metformina (51 %), una combinación de metformina e insulina (40,1 %) insulina (3,2 %) o ninguno (5,7 %).
El cambio medio ajustado de la HbA1c en la semana 26 entre empagliflozina (N = 52) y placebo (N = 53) de -0,84 % fue clínicamente importante y estadísticamente significativo (IC del 95 % -1,50, -0,19; p = 0,0116). Además, el tratamiento con empagliflozina en comparación con placebo produjo un cambio medio ajustado clínicamente importante de la GPA de -35,2 mg/dl (IC del 95 % -58,6, -11,7) (-1,95 mmol/l [-3,25, -0,65]).
Insuficiencia cardíaca y enfermedad renal crónica
La Agencia Europea de Medicamentos ha eximido al titular de la obligación de presentar los resultados de los ensayos realizados con Jardiance en todos los grupos de la población pediátrica en la insuficiencia cardíaca y en el tratamiento de la enfermedad renal crónica (ver sección 4.2 para consultar la información sobre el uso en la población pediátrica).
 5.2 - Propiedades farmacocinéticas de JARDIANCE 25 mg Comp. recub. con película
5.2 - Propiedades farmacocinéticas de JARDIANCE 25 mg Comp. recub. con película
Absorción
La farmacocinética de empagliflozina se ha caracterizado extensivamente en voluntarios sanos y en pacientes con diabetes tipo 2. Tras la administración oral, empagliflozina se absorbió rápidamente, alcanzándose concentraciones plasmáticas máximas a una mediana de tmax de 1,5 horas después de la dosis. Después, las concentraciones plasmáticas disminuyeron de forma bifásica con una fase de distribución rápida y una fase terminal relativamente lenta. La AUC plasmática media en estado estacionario y la Cmax fueron de 1 870 nmol.h/l y 259 nmol/l con empagliflozina 10 mg y de 4 740 nmol.h/l y 687 nmol/l con empagliflozina 25 mg una vez al día. La exposición sistémica de empagliflozina aumentó de forma proporcional a la dosis. Los parámetros farmacocinéticos de dosis única y de estado estacionario de empagliflozina fueron similares, lo que sugiere una farmacocinética lineal respecto al tiempo. No hubo diferencias clínicamente relevantes en la farmacocinética de empagliflozina entre los voluntarios sanos y los pacientes con diabetes tipo 2.
La administración de empagliflozina 25 mg después de la ingesta de una comida rica en grasas y alta en calorías dio lugar a una exposición ligeramente inferior; la AUC disminuyó en aproximadamente el 16 % y la Cmax disminuyó en aproximadamente un 37 % en comparación con las condiciones de ayunas. El efecto observado de los alimentos sobre la farmacocinética de empagliflozina no se consideró clínicamente relevante, por lo que empagliflozina puede administrarse con o sin alimentos.
Distribución
En base al análisis farmacocinético poblacional, se calculó que el volumen de distribución aparente en estado estacionario era de 73,8 litros. Después de la administración de una solución oral de [14C]-empagliflozina a voluntarios sanos, la distribución de los glóbulos rojos fue de aproximadamente un 37 % y la unión a proteínas plasmáticas del 86 %.
Biotransformación
No se detectaron metabolitos importantes de empagliflozina en el plasma humano y los metabolitos más abundantes fueron tres conjugados glucurónidos (2-, 3- y 6-O glucurónido). La exposición sistémica de cada metabolito fue inferior al 10 % del material total relacionado con el fármaco. Los estudios in vitro sugirieron que la principal vía metabólica de empagliflozina en humanos es la glucuronidación por las uridina 5'-difosfo-glucuronosiltransferasas UGT2B7, UGT1A3, UGT1A8 y UGT1A9.
Eliminación
En base al análisis farmacocinético poblacional, se calculó que la semivida de eliminación terminal aparente de empagliflozina era de 12,4 horas y que el aclaramiento oral aparente era de 10,6 l/hora. Las variabilidades interindividual y residual para el aclaramiento oral de empagliflozina fueron del 39,1 % y del 35,8 %, respectivamente. Con una pauta posológica de una vez al día, las concentraciones plasmáticas de empagliflozina en estado estacionario se alcanzaron en la quinta dosis. Acorde con la semivida, en el estado estacionario se observó una acumulación de hasta el 22 % con respecto al AUC plasmática. Tras la administración de una solución oral de [14C]-empagliflozina a voluntarios sanos, aproximadamente el 96 % de la radioactividad relacionada con el fármaco se eliminó por las heces (41 %) o la orina (54 %). La mayor parte de la radioactividad relacionada con el fármaco que se recuperó en las heces fue el fármaco original sin cambios y aproximadamente la mitad de la radioactividad relacionada con el fármaco excretado por la orina fue el fármaco original sin cambios.
Poblaciones especiales
Insuficiencia renal
En pacientes con insuficiencia renal leve, moderada o grave (TFGe <30 - <90 ml/min/1,73 m2) y pacientes con fallo renal/enfermedad renal terminal (ERT), el AUC de empagliflozina aumentó en aproximadamente el 18 %, 20 %, 66 % y 48 % respectivamente en comparación con los sujetos con una función renal normal. Los niveles plasmáticos máximos de empagliflozina fueron similares en los sujetos con insuficiencia renal moderada y fallo renal/ERT en comparación con los pacientes con una función renal normal. Los niveles plasmáticos máximos de empagliflozina fueron aproximadamente un 20 % más altos en los sujetos con insuficiencia renal leve y grave en comparación con los sujetos con una función renal normal. El análisis farmacocinético poblacional demostró que el aclaramiento oral aparente de empagliflozina disminuía con un descenso en la TFGe, dando lugar a un aumento en la exposición al fármaco.
Insuficiencia hepática
En sujetos con insuficiencia hepática leve, moderada y grave según la clasificación Child-Pugh, el AUC de empagliflozina aumentó en aproximadamente el 23 %, 47 %, y 75 % y la Cmax aumentó en el 4 %, 23 % y 48 % respectivamente en comparación con los sujetos con función hepática normal.
Índice de masa corporal
El índice de masa corporal no tuvo ningún efecto clínicamente relevante sobre la farmacocinética de empagliflozina según un análisis farmacocinético poblacional. En este análisis, se estimó que el AUC era un 5,82 %, 10,4 % y 17,3 % inferior en sujetos con un IMC de 30, 35 y 45 kg/m2 respectivamente, en comparación con sujetos con un índice de masa corporal de 25 kg/m2.
Sexo
El sexo no tuvo ningún efecto clínicamente relevante sobre la farmacocinética de empagliflozina según un análisis farmacocinético poblacional.
Raza
En el análisis farmacocinético poblacional, se estimó que el AUC era un 13,5 % más alta en asiáticos con un índice de masa corporal de 25 kg/m2 en comparación con los no asiáticos con un índice de masa corporal de 25 kg/m2.
Pacientes de edad avanzada
La edad no tuvo ningún efecto clínicamente relevante sobre la farmacocinética de empagliflozina según un análisis farmacocinético poblacional.
Población pediátrica
Un estudio pediátrico de fase I examinó la farmacocinética y la farmacodinámica de empagliflozina (5 mg, 10 mg y 25 mg) en niños y adolescentes de ≥10 a <18 años de edad con diabetes mellitus tipo 2. Las respuestas farmacocinéticas y farmacodinámicas observadas concordaban con las obtenidas en sujetos adultos.
Un estudio pediátrico de fase III examinó la farmacocinética y la farmacodinámica (cambio de la HbA1c desde el momento inicial) de empagliflozina 10 mg con un posible aumento de dosis a 25 mg en niños y adolescentes de 10 a 17 años de edad con diabetes mellitus tipo 2. La relación exposición-respuesta observada fue en conjunto comparable en adultos y en niños y adolescentes. La administración oral de empagliflozina dio lugar a una exposición dentro del intervalo observado en pacientes adultos.
La media geométrica de las concentraciones mínimas y la media geométrica de las concentraciones observadas 1,5 horas después de la administración en estado estacionario fueron de 26,6 nmol/l y 308 nmol/l con empagliflozina 10 mg una vez al día y de 67,0 nmol/l y 525 nmol/l con empagliflozina 25 mg una vez al día.
 5.3 - Datos preclínicos sobre seguridad de JARDIANCE 25 mg Comp. recub. con película
5.3 - Datos preclínicos sobre seguridad de JARDIANCE 25 mg Comp. recub. con película
Los datos de los estudios preclínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, genotoxicidad, fertilidad y desarrollo embrionario temprano.
En estudios de toxicidad a largo plazo con roedores y perros, se observaron signos de toxicidad a exposiciones iguales o superiores a 10 veces la dosis clínica de empagliflozina. La mayor parte de las toxicidades fueron compatibles con la farmacología secundaria relacionada con pérdida de glucosa por la orina y desequilibrios electrolíticos, incluida la disminución del peso y la grasa corporales, aumento del consumo de alimentos, diarrea, deshidratación, disminución de los niveles de glucosa sérica y aumentos en otros parámetros séricos que reflejan el aumento del metabolismo de las proteínas y la gluconeogénesis, cambios urinarios como la poliuria y la glucosuria y cambios microscópicos, incluida la mineralización en el riñón y en algunos tejidos blandos y vasculares. Las evidencias microscópicas de los efectos de una farmacología exagerada en el riñón que se observaron en algunas especies incluyeron dilatación tubular y mineralización tubular y pélvica a aproximadamente 4 veces la exposición del AUC clínica de empagliflozina asociada a la dosis de 25 mg.
Empagliflozina no es genotóxica.
En un estudio de carcinogenicidad de 2 años de duración, empagliflozina no aumentó la incidencia de tumores en ratas hembra hasta la dosis máxima de 700 mg/kg/día, lo que corresponde a aproximadamente 72 veces la exposición clínica máxima del AUC a empagliflozina. En las ratas macho, a las dosis más altas se observaron lesiones proliferativas vasculares benignas relacionadas con el tratamiento (hemangiomas) del ganglio linfático mesentérico, pero no a la dosis de 300 mg/kg/día, lo que corresponde a aproximadamente 26 veces la exposición clínica máxima a empagliflozina. Se observaron tumores celulares intersticiales en los testículos con una mayor incidencia en ratas a 300 mg/kg/día o más, pero no a 100 mg/kg/día, lo que corresponde a aproximadamente 18 veces la exposición clínica máxima a empagliflozina. Ambos tumores son frecuentes en ratas, pero es improbable que sean relevantes en los humanos.
Empagliflozina no aumentó la incidencia de tumores en ratones hembra a dosis de hasta 1 000 mg/kg/día, lo que corresponde a aproximadamente 62 veces la exposición clínica máxima a empagliflozina. Empagliflozina indujo tumores renales en ratones macho a dosis de 1 000 mg/kg/día, pero no a la dosis de 300 mg/kg/día, lo que corresponde a aproximadamente 11 veces la exposición clínica máxima a empagliflozina. El modo de acción de estos tumores depende de la predisposición natural del ratón macho a presentar una patología renal y una vía metabólica que no refleja la de los humanos. Los tumores renales de los ratones macho no se consideran relevantes para los humanos.
A exposiciones suficientemente superiores a la exposición en humanos después de dosis terapéuticas, empagliflozina no tuvo efectos adversos sobre la fertilidad o el desarrollo embrionario temprano. La administración de empagliflozina durante el periodo de organogénesis no fue teratogénica. Solo a dosis tóxicas para la madre, empagliflozina también provocó que los huesos de las extremidades de la rata se doblasen, así como un aumento de la muerte embriofetal en el conejo.
En estudios de la toxicidad prenatal y posnatal en ratas, se observó una reducción en el aumento de peso de la descendencia a exposiciones maternas de aproximadamente 4 veces la exposición clínica máxima a empagliflozina. Dicho efecto no se observó a la exposición sistémica igual a la máxima exposición clínica a empagliflozina. La relevancia de este hallazgo para los humanos no está clara.
En un estudio de toxicidad juvenil en ratas, cuando se administró empagliflozina desde el día 21 posnatal hasta el día 90 posnatal, se observó una dilatación pélvica y de los túbulos renales, no adversa y de mínima a leve, en ratas jóvenes solo a 100 mg/kg/día, lo que se aproxima a 11 veces la dosis clínica máxima de 25 mg. Estos hallazgos no estaban presentes tras un periodo de recuperación de 13 semanas sin fármaco.
 6. - DATOS FARMACÉUTICOS
6. - DATOS FARMACÉUTICOS
 6.1 - Lista de excipientes de JARDIANCE 25 mg Comp. recub. con película
6.1 - Lista de excipientes de JARDIANCE 25 mg Comp. recub. con película
Núcleo del comprimido
Lactosa monohidrato
Celulosa microcristalina
Hidroxipropilcelulosa
Croscarmelosa sódica
Sílice coloidal anhidra
Estearato de magnesio
Cubierta pelicular
Hipromelosa
Dióxido de titanio (E171)
Talco
Macrogol (400)
Óxido de hierro amarillo (E172)
 6.2 - Incompatibilidades de JARDIANCE 25 mg Comp. recub. con película
6.2 - Incompatibilidades de JARDIANCE 25 mg Comp. recub. con película
No procede.
 6.3 - Período de validez de JARDIANCE 25 mg Comp. recub. con película
6.3 - Período de validez de JARDIANCE 25 mg Comp. recub. con película
3 años
 6.4 - Precauciones especiales de conservación de JARDIANCE 25 mg Comp. recub. con película
6.4 - Precauciones especiales de conservación de JARDIANCE 25 mg Comp. recub. con película
No requiere condiciones especiales de conservación.
 6.5 - Naturaleza y contenido del recipiente de JARDIANCE 25 mg Comp. recub. con película
6.5 - Naturaleza y contenido del recipiente de JARDIANCE 25 mg Comp. recub. con película
Blísteres unidosis perforados de PVC/aluminio.
Tamaños de envases de 7 x 1, 10 x 1, 14 x 1, 28 x 1, 30 x 1, 60 x 1, 70 x 1, 90 x 1, y 100 x 1 comprimidos recubiertos con película.
Puede que solamente estén comercializados algunos tamaños de envases.
 6.6 - Precauciones especiales de eliminación y otras manipulaciones de JARDIANCE 25 mg Comp. recub. con película
6.6 - Precauciones especiales de eliminación y otras manipulaciones de JARDIANCE 25 mg Comp. recub. con película
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
 7. - TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
7. - TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Boehringer Ingelheim International GmbH
Binger Str. 173
55216 Ingelheim am Rhein
Alemania
 8. - NÚMERO(S) DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
8. - NÚMERO(S) DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Jardiance 10 mg comprimidos recubiertos con película
EU/1/14/930/010
EU/1/14/930/011
EU/1/14/930/012
EU/1/14/930/013
EU/1/14/930/014
EU/1/14/930/015
EU/1/14/930/016
EU/1/14/930/017
EU/1/14/930/018
Jardiance 25 mg comprimidos recubiertos con película
EU/1/14/930/001
EU/1/14/930/002
EU/1/14/930/003
EU/1/14/930/004
EU/1/14/930/005
EU/1/14/930/006
EU/1/14/930/007
EU/1/14/930/008
EU/1/14/930/009
 9. - FECHA DE LA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
9. - FECHA DE LA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 22/mayo/2014
Fecha de la última renovación: 14/febrero/2019
 10. - FECHA DE LA REVISIÓN DEL TEXTO
10. - FECHA DE LA REVISIÓN DEL TEXTO
07/diciembre/2023
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.