Informe de Posicionamiento Terapéutico de vemurafenib (Zelboraf®)
INFORME DE POSICIONAMIENTO TERAPÉUTICO PT/V1/15112013.2
Informe de Posicionamiento Terapéutico de Vemurafenib (Zelboraf ® )
Fecha de publicación: 22 de noviembre de 2013
La tasa ajustada de incidencia de melanoma en España oscila entre 5,3 y 5,8 por cada 100.000 habitantes/año (1). La mitad de los casos, aproximadamente, afecta al grupo de edad comprendido entre los 35 y 65 años, con una mediana de edad en el momento del diagnóstico de 57 años. La incidencia se ha visto incrementada en las últimas décadas de manera continua y afecta a todas las edades (2).
Cerca de un 40% de los pacientes con melanoma desarrollan un estadio avanzado de la enfermedad (III ó IV) si bien en nuestro país este dato parece ser menor a tenor de una tasa de muerte de entre un 20-25% (3). El tratamiento establecido para el melanoma avanzado incluye cirugía, radioterapia y/o terapia sistémica. La resección total de metástasis aisladas y restringidas a un único lugar anatómico puede, en algunos casos, prolongar significativamente la supervivencia. La radioterapia paliativa estaría indicada en el alivio sintomático de las metástasis cerebrales, tejido óseo y vísceras. La terapia sistémica consiste en la administración de inmunoterapia [Ipilimumab, interleukina-2 (IL-2) (uso muy limitado)] o quimioterapia (dacarbazina, temozolomida, fotemustina, platinos y taxanos o la combinación de estos). Posteriormente a la autorización de vemurafenib, se ha autorizado dabrafenib para el tratamiento en monoterapia de pacientes adultos con melanoma no resecable o metastásico con mutación BRAF V600.
El gen BRAF (V-RAF homólogo B1 del oncogén viral del sarcoma murino), es la mutación más frecuente en el melanoma cutáneo y está presente en aproximadamente un 50% de los melanomas. Las mutaciones oncogénicas en BRAF provocan una activación de la ruta RAF-MEK-ERK estimulando la proliferación celular. Las mutaciones BRAF observadas más frecuentemente en melanoma parecen ser las V600E (74-90%), V600K (15-25%), V600R y V600D (4). La más frecuente se produce por una sustitución de valina por ácido glutámico en la posición 600 BRAF (V600E); las mutaciones menos frecuentes comprenden valina 600 a residuos de lisina o arginina (V600K/R).
VEMURAFENIB (ZELBORAF®)
Vemurafenib ha sido autorizado en monoterapia para el tratamiento de pacientes adultos con melanoma no resecable o metastásico con mutación de BRAF V600 positiva (5).
Vemurafenib se presenta en comprimidos recubiertos con película. Cada comprimido contiene 240 mg de vemurafenib.
La dosis recomendada de vemurafenib es de 960 mg (4 comprimidos de 240 mg) dos veces al día. Vemurafenib puede tomarse con o sin alimentos, pero debe evitarse el consumo constante de las dos dosis diarias con el estómago vacío.
Antes de comenzar el tratamiento con vemurafenib, los pacientes deben tener un diagnóstico de mutación BRAF V600 positiva en el tumor, confirmado por un test validado.
El tratamiento con vemurafenib debe continuarse hasta la progresión de la enfermedad o hasta que aparezca una toxicidad no aceptable.
Farmacología
Vemurafenib es un inhibidor de la serina-treonina cinasa BRAF que actúa evitando la proliferación celular que tiene lugar en ausencia de los factores de crecimiento que normalmente son requeridos para la proliferación. Vemurafenib es un fármaco de baja solubilidad y permeabilidad.
Se dispone de un total de 7 estudios clínicos para avalar la eficacia y seguridad (incluyendo farmacocinética) de vemurafenib: cinco estudios fase I, un estudio fase II y el estudio pivotal fase III (6).
Eficacia
La eficacia de vemurafenib ha sido evaluada en 337 pacientes de un ensayo clínico fase III (BRIM3 o NO25026) y en 132 pacientes incluidos en un ensayo clínico fase II (BRIM2 o NP22657). Todos los pacientes debían estar diagnosticados de melanoma avanzado con mutación BRAF V600E (de acuerdo al Test de Mutación V600 cobas 4800).
La dosis propuesta para el estudio pivotal (960 mg administrados dos veces al día, BID) fue seleccionada teniendo en cuenta los datos preclínicos y los resultados del estudio fase I PLX06-0 de búsqueda de dosis.
El estudio BRIM3 fue un ensayo multicéntrico, aleatorizado y abierto, en el que se comparó vemurafenib versus dacarbazina en 1ª línea de pacientes con melanoma metastásico o no resecable (5-7).
Según los principales criterios de inclusión/exclusión, los pacientes incluidos en el estudio fueron sujetos sin tratamiento previo para enfermedad avanzada con melanoma (V600E) estadio IIIc o IV no resecable e histológicamente confirmado. Además se requirió un estado funcional en la escala de actividad del grupo oncológico cooperativo (ECOG) de 0-1 y una expectativa de vida mayor de 3 meses. Se excluyeron pacientes con lesiones activas en sistema nervioso central, con excepción de aquellos con metástasis cerebrales controladas al menos 3 meses después de completar terapia local (cirugía o estereotaxia) y no estuvieran recibiendo corticoides durante más de 3 semanas.
La supervivencia libre de progresión (SLP) y la supervivencia global (SG) fueron ambas co-variables primarias del estudio, si bien inicialmente el objetivo primario fue SG. Como variables secundarias se incluyeron la mejor tasa de respuesta global ("best objective response rate”, BORR por sus siglas en inglés), tiempo hasta la respuesta y duración de la respuesta. La evaluación de la progresión del tumor no la realizó un comité independiente ciego al tratamiento, como es deseable en estos estudios.
Un total de 675 pacientes fueron aleatorizados (1:1) a dacarbazina (n=338), 1000 mg/m2 cada 3 semanas, o al grupo de vemurafenib (n=337), 960 mg dos veces al día. El estudio se llevó a cabo en 104 centros de 12 países. Se estratificó en función de la región geográfica (Norteamérica, Europa occidental, Australia/Nueva Zelanda, otros), ECOG (0,1), estadio (IIIC, M1a, M1b, M1c) y niveles de lactato deshidrogenasa (LDH normal, elevada).
La mayoría de los pacientes que recibieron vemurafenib fueron varones (56%) y de raza caucásica (99%), con una edad media de 54 años (un 24% fueron ≥ 65 años). Todos los pacientes tenían un estado dentro de la escala ECOG de 0 ó 1 (68% ECOG 0), y la mayoría de los pacientes (65%) tenían un estadio M1c de la enfermedad con solo un 5% en estadio IIIC. No se observaron diferencias significativas entre grupos en las variables basales demográficas, factores de riesgo y características de la enfermedad. Un total de 57 de los 673 pacientes (8,46%) cuyos tumores fueron analizados retrospectivamente por secuenciación, mostraron tener melanoma con mutación positiva BRAF V600K en el ensayo BRIM3.
En un análisis intermedio pre-especificado con fecha de corte de 30 de diciembre de 2010, se observó una mejoría significativa en las variables principales del ensayo de SG (p<0,0001) y SLP (p<0,0001) (test de log-rank no estratificado) (38% de eventos para vemurafenib y 66% para dacarbazina). La recomendación del Comité de Monitorización de Datos de Seguridad (Upon Data Safety Monitoring Board, DSMB) fue que estos resultados se liberaran en enero de 2011 y que se modificara el estudio para permitir que los pacientes con dacarbazina se cruzaran al grupo de vemurafenib.
El porcentaje de pacientes vivos al año (datos obtenidos en octubre 2011) fue de un 55% y 43% para vemurafenib y dacarbazina respectivamente.
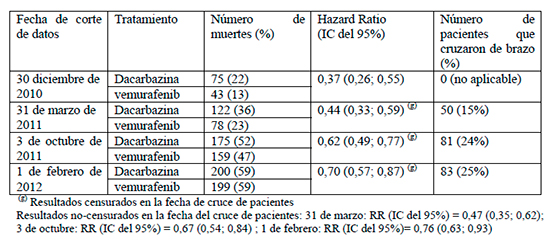
En un análisis con datos más maduros, los resultados de SG a fecha de febrero de 2012 mostraron un reducción del riesgo de muerte del 30 % [HR 0,70 IC95% (0,57; 0,87)] tras la censura de los 83 pacientes del grupo de dacarbazina (DTIC) que se cruzaron al grupo de tratamiento con vemurafenib, y de un 24% [HR 0,76 IC95%(0,63; 0,93)] sin aplicar censuras por cruce de brazo de tratamiento. Las medianas de supervivencia ofrecen una ganancia estimada de 3,9 meses (13,6 y 9,7 meses de SG para vemurafenib y dacarbazina respectivamente).
Los resultados en términos de SLP mostraron a fecha de febrero de 2012 una reducción del riesgo de progresión o muerte del 62% [HR 0,38 IC95%(0,32; 0,46)] con unas medianas de 6,87 meses y 1,64 meses para vemurafenib y dacarbazina, respectivamente.
La tasa de respuesta global de vemurafenib fue del 48,4% vs. 5,5% en dacarbazina.
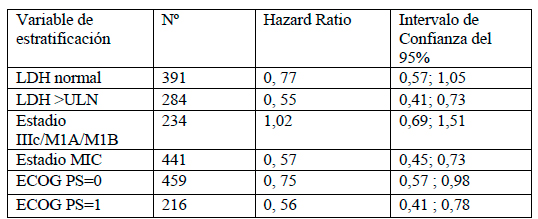
En el análisis de subgrupos, la variable de supervivencia global mostró, de manera general, la solidez de los datos, si bien, los estratos de estadio de la enfermedad, estado funcional y nivel de LDH mostraron resultados dispares. Particularmente en el estrato de los pacientes con estadio IIIC/M1A/M1B (n=234), el resultado no parece beneficiar el tratamiento con vemurafenib en términos de SG (HR=1,02; IC95% 0,69-1,51).
Los análisis de eficacia en pacientes con tumores V600K- positivo sugirieron un beneficio similar del tratamiento con vemurafenib. Se observó una tendencia positiva en SG (HR= 0.27; IC95% 0.17-1.15; n=19) y un resultado positivo en SLP (HR=0.09; IC95% 0.02-0.45; n=19).
Se evaluó la calidad de vida mediante cuestionarios FACT-M (Functional Assessment of Cancer Therapy-Melanoma). El análisis de estos cuestionarios sugirió que no había evidencia que indicara diferencias respecto a la calidad de vida en los diferentes grupos de tratamiento, si bien debido al número de pacientes y al diseño abierto del estudio, no se puede concluir sobre la influencia de vemurafenib en la calidad de vida del paciente.
Además del estudio pivotal BRIM3, se presentaron los resultados del estudio BRIM2 (NP 22657) un ensayo abierto, de un solo brazo, de fase II, en el que se evaluó la eficacia y seguridad de vemurafenib en pacientes con melanoma metastásico y estado mutacional BRAF V600E, que habían sido tratados previamente (6,8). Concretamente, se incluyeron pacientes con diagnóstico de melanoma irresecable grado IV, positivo al test de la mutación BRAF V600E, edad ≥ 18 años, progresión de la enfermedad con al menos un tratamiento sistémico previo para enfermedad avanzada (incluida la IL-2 y la quimioterapia estándar), ECOG 0-1, metástasis cerebrales controladas al menos 3 meses después de completar terapia local, sin otro cáncer invasivo en los 5 últimos años y función hematológica, hepática y renal adecuada. Se reclutó un total de 132 pacientes.
La variable principal del estudio fue BORR de acuerdo a la evaluación de un comité independiente. Como principales variables secundarias se incluyeron BORR según el investigador, SLP, tiempo hasta la respuesta y SG.
Con una mediana de seguimiento de 12,9 meses (rango 0,6 - 20,1), el porcentaje de pacientes que alcanzó la variable principal fue del 53% (IC del 95%: 44%, 62%). La mediana de la supervivencia global fue de 15,9 meses (IC del 95%: 11,6; 18,3). La tasa de supervivencia global a los 6 meses fue del 77% (IC del 95%: 70%, 85%) y a los 12 meses fue 58% (IC del 95%: 49%, 67%).
Nueve de los 132 (6,8%) pacientes reclutados en el ensayo BRIM2 tuvieron tumores con mutación V600K positiva. Entre estos pacientes, 3 tuvieron una respuesta parcial (RP), 3 tuvieron enfermedad estable (EE), 2 tuvieron progresión de la enfermedad (PE) y uno no fue evaluable.
Seguridad
Los datos de seguridad se basan fundamentalmente en 635 pacientes que recibieron al menos una dosis de vemurafenib, de los que 581 fueron tratados con 960 mg dos veces al día.
El estudio pivotal BRIM 3 se considera la principal fuente de datos para la población diana, sirviendo de apoyo los del estudio BRIM2 y los demás estudios en fase I.
La duración media de tratamiento fue de 3.1 meses para el grupo de vemurafenib y de 0.76 meses para los pacientes tratados con dacarbazina, con un número medio de ciclos de 2 (1000 mg/m2 por ciclo).
Un total de 147 pacientes (44%) interrumpió al menos una dosis de vemurafenib, con una media de 2 interrupciones por paciente. Durante el estudio fue necesario modificar la dosis a 159 sujetos (47%). A 112 se les redujo la dosis (reducción a 720 mg BID en el 74% de los pacientes, y a 480 mg BID en el 23%). Al menos 129 pacientes del brazo de vemurafenib necesitaron una reducción o interrupción de la dosis debida a una reacción adversa.
Las reacciones adversas más comunes (RA) (> 30%) notificadas con vemurafenib durante todo su desarrollo, incluyen artralgia, astenia, rash, reacciones de fotosensibilidad, náuseas, alopecia y prurito. Se notificó de manera muy frecuente (20%) carcinoma de células escamosas cutáneo (CCEc) que en la mayoría de los casos fue tratado mediante extirpación local.
Un porcentaje mayor de pacientes experimentaron reacciones adversas de grado 3 o superior en el grupo de vemurafenib (50% vs 30%). Las reacciones adversas grado 3 descritas más frecuentemente incluyen CCEc y rash. Las reacciones adversas de grado 4 fueron más frecuentes en el grupo de dacarbazina (8%) que en el brazo de vemurafenib (4%). Entre las reacciones adversas de grado 4 descritas para vemurafenib se describieron: embolia pulmonar, incremento de los niveles de GGT (gamma glutamil transferasa), fosfatasa alcalina, bilirrubina y lipasa, ageusia, hemorragia intraventricular, neumonía, neumotórax y neutropenia.
Entre las reacciones adversas de especial interés se describieron el aumento de las enzimas hepáticas, CCEc, carcinoma de células escamosas no cutáneo, nuevo melanoma primario, reacciones de hipersensibilidad y dermatológicas y por último prolongación del intervalo QT.
En resumen, parece ser que piel, sistema gastrointestinal y musculoesquelético y tejido conectivo son los órganos diana en toxicidad.
DISCUSIÓN
El tratamiento de primera línea del melanoma metastásico incluye actualmente la monoterapia con dacarbazina (tratamiento de referencia), y en menor medida temozolomida, fotemustina, carboplatino y su combinación con paclitaxel e interleukina 2 (IL2).
En relación a la segunda línea de tratamiento, Ipilimumab ha sido autorizado para el tratamiento del melanoma avanzado (irresecable o metastásico) en adultos que ya han recibido tratamiento anteriormente, si bien tal y como recoge el IPT de ipilimumab (9) para maximizar la eficiencia del tratamiento, deberá tenerse en cuenta la expectativa de supervivencia del paciente, el estado funcional, la presencia de otras comorbilidades, y el número de líneas de tratamiento recibidas previamente. Además de ipilimumab en segunda línea, también existen datos de la combinación de carboplatino/paclitaxel (10-12) si bien su uso no parece estar muy extendido en nuestro país pese a los datos publicados de eficacia. Los resultados del estudio principal BRIM3, tanto en términos de SG como en SLP, se consideran clínicamente relevantes.
La ganancia de aproximadamente 5 meses en SLP y de 4 meses de SG respecto a dacarbazina se traducen en una mediana de esperanza de vida de 13 meses y medio, con una reducción del riesgo de muerte de un 30% y una supervivencia a los 12 meses del 55% en comparación con 43% de dacarbazina (valor que incluye un porcentaje importante de pacientes de dacarbazina (25%) que pasaron a recibir vemurafenib).
Analizando en detalle los datos del estudio pivotal de vemurafenib y más concretamente los diferentes estratos en que fueron aleatorizados los pacientes, se ve cómo los resultados de la variable SG parecen mejores en aquellos sujetos con peor pronóstico (ECOG PS=1, LDH>ULN y especialmente aquellos con estadio M1c vs. estadio III, M1a;M1b) –ver tabla-.
Esta idea de que vemurafenib sería más eficaz en aquellos pacientes con peor expectativa, parece reforzarse por los datos de SG en la población ITT del estudio. Así, tal y como puede observarse en las distintas actualizaciones de los resultados de SG, según se alcanzan mayor número de eventos, el Hazard Ratio se incrementa paulatinamente, llegando a 0,70, que si bien es todavía considerado clínicamente relevante, intuitivamente sugiere que el beneficio en los pacientes con una progresión más lenta de la enfermedad sería menor. Este hecho podría explicarse en parte por el cruce de pacientes al brazo de vemurafenib, si bien, al observar los datos de SG censurando los pacientes inicialmente aleatorizados en el brazo dacarbazina pero que recibieron tratamiento con vemurafenib, no parece existir una gran diferencia entre los HR (HR=0.70 vs. HR=0.76).
Otra explicación a la posible menor eficacia de vemurafenib en aquellos pacientes con mejor pronóstico, sería que los datos de los estratos con peor HR no tuvieran en el momento del análisis una suficiente madurez, y que por tanto ese menor número de eventos estuviese provocando unos resultados artificialmente peores. No obstante, es llamativo el hecho de que el HR para el estrato de pacientes en estadio IIIC/M1A/M1B haya aumentado en la medida que se incrementa el número de eventos, pasando de 0.64 a 0.94 en penúltima actualización, a 1.02 en la última. Ciertamente, puede existir una sobrerrepresentación de pacientes que cambiaron de brazo de tratamiento en estos estadios, si bien la diferencia en términos de HR en la penúltima actualización de los datos de SG no es muy relevante (HR=0.94 vs HR=0.87).
Por ello, teniendo en cuenta las limitaciones de los análisis por subgrupos, pero admitiendo también la estratificación por estadio de enfermedad y la consiguiente minimización de los posibles sesgos debido a diferencias basales en la aleatorización, la relevancia clínica del efecto mostrado por el tratamiento con vemurafenib podría ser menor en aquellos pacientes con un mejor pronóstico en base al estadio de la enfermedad (IIIC/M1A/M1B) y en menor medida al estado funcional del paciente y niveles de LDH. En cualquier caso es necesario realizar nuevos análisis o futuros estudios que nos sirvan para comprobar si realmente hay subgrupos de pacientes con melanoma metastásico o no resecable que puedan beneficiarse más que otros o bien si estos resultados fueron motivados por el cruce de pacientes entre brazos y/o la inmadurez en los resultados del ensayo clínico a día de hoy.
No se detectan diferencias en términos de SLP entre los diferentes estratos de la aleatorización. Estos resultados podrían ser explicables por el bajo número de eventos observados ([66% (n=182) vs 38% (n=104)] dacarbazina y vemurafenib respectivamente).
Con relación a la influencia que el tipo de mutación BRAF V600 pueda tener en la eficacia, cabe señalar que pese al pequeño tamaño de muestra de los pacientes con mutación V600K, se puede intuir un beneficio para estos pacientes tanto en SG como en SLP. Además, los datos preclínicos parecen respaldar los resultados en pacientes con mutaciones distintas a V600E. Vemurafenib parece inhibir distintos subtipos de mutaciones BRAF, como V600D, V600K y V600R. Por último, estudios "in vitro" muestran la actividad inhibitoria de vemurafenib a concentraciones sub-micromolar, las cuales estarían por debajo de las alcanzadas "in vivo". Por todo ello, parece razonable esperar actividad en mutaciones distintas a las V600E.
La indicación autorizada de vemurafenib es el tratamiento en monoterapia de pacientes adultos con melanoma no resecable o metastásico con mutación de BRAF V600 positiva, tanto en primera como en segunda línea. Los datos de eficacia en segunda línea de tratamiento provienen del estudio BRIM2, el cual mostró una mediana de supervivencia de 15.9 meses con un porcentaje de supervivencia a los 12 meses del 58%, si bien dado el carácter no comparativo del estudio y el tamaño de la muestra, obliga a tomar con cierta cautela los hallazgos encontrados en esta población.
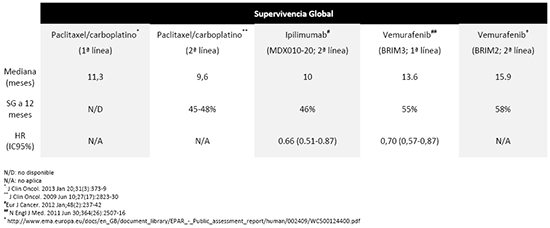
Comparando estos datos con aquellos obtenidos por ipilimumab y con la combinación de paclitaxel/carboplatino (10-12) (ver tabla al final del informe) se intuye, en primer lugar, que la actividad de vemurafenib es independiente de la línea de tratamiento y en segundo lugar, que pese a las limitaciones del estudio y de la comparación, vemurafenib podría proporcionar, en el peor escenario, un beneficio comparable a ipilimumab y paclitaxel/carboplatino, si no quizá una mayor eficacia. Todo ello asumiendo que tanto ipilimumab como la combinación de paclitaxel/carboplatino otorga un aumento de la supervivencia independientemente del estado mutacional del BRAF. (10-14).
También es importante señalar que las comparaciones indirectas asumidas, metodológicamente no son las idóneas. En segunda línea los resultados del ensayo de vemurafenib corresponden a un estudio fase II sin grupo control (6,8); Los resultados del ensayo de ipilimumab corresponden a un estudio fase III que compara el empleo de ipilimumab en monoterapia frente a vacuna gp100 (14- 16); Los resultados del ensayo de carboplatino/paclitaxel corresponden a un fase III que compara la asociación carboplatino/paclitaxel más placebo frente a la asociación carboplatino/paclitaxel más sorafenib (11).
En primera línea de tratamiento la comparación se realizaría con los resultados obtenidos del ensayo de vemurafenib fase III en el que se compara el fármaco con el grupo de control dacarbazina (7) con los resultados del estudio fase III que compara la asociación carboplatino/paclitaxel más placebo frente a la asociación carboplatino/paclitaxel más sorafenib (10).
Ante lo expuesto, es indiscutible que se necesitarían ensayos comparativos directos para poder obtener conclusiones válidas y definitivas en cuanto a eficacia y seguridad comparada.
Merece también atención el posible uso de vemurafenib en pacientes con metástasis cerebrales. La información sobre el balance beneficio riesgo del tratamiento con vemurafenib en esta población no puede extraerse del estudio pivotal, ya que estos pacientes fueron excluidos en líneas generales del estudio. Actualmente se encuentra en marcha un estudio fase II, de un solo brazo, para evaluar la eficacia de vemurafenib en pacientes con afectación del SNC (NCT01378975). No obstante, son varios los estudios que han investigado la eficacia y seguridad de vemurafenib en esta población de especial mal pronóstico, llegando todos ellos a la conclusión que existe actividad antitumoral en estos pacientes. Con todo, pese a no disponer de resultados con el máximo nivel de evidencia, parece razonable asumir cierto nivel de eficacia en esta población. (17)
No hubo pacientes con melanoma ocular en los estudios, si bien aún con cierta incertidumbre es esperable actividad antitumoral en los mismos.
Por último, se ha propuesto que una asociación entre ipilimumab y vemurafenib podría otorgar mayores ventajas a los pacientes con melanoma metastásico. Si bien a priori existe plausibilidad biológica sobre esta asociación, esta asociación no es recomendable dado que los únicos datos publicados de la combinación de vemurafenib e ipilimumab señalan graves problemas de hepatotoxicidad, los cuales llevaron a la paralización de dicho estudio (18).
CONCLUSIÓN
Vemurafenib ha demostrado un beneficio clínicamente significativo en el tratamiento de pacientes adultos con melanoma no resecable o metastásico con mutación de BRAF V600 positiva.
Con objeto de maximizar la eficiencia del tratamiento, deberá tenerse en cuenta: la expectativa de supervivencia del paciente (una expectativa no inferior a 3 meses fue criterio de entrada en el ensayo clínico) y el estado funcional (ECOG 0-1 como criterio de entrada al ensayo clínico) si bien, la decisión de tratamiento a pacientes fuera de estas recomendaciones generales debería ser considerada de manera individualizada.
Según los datos actuales, y considerando las limitaciones de comparaciones indirectas, parece que vemurafenib podría ser similar o superior en eficacia a ipilimumab o paclitaxel/carboplatino.
Según los estudios de vemurafenib en pacientes con metástasis en el sistema nervioso central y pese a no disponer de resultados con el máximo nivel de evidencia, parece razonable asumir cierto nivel de eficacia en esta población.
No ha de administrarse simultáneamente con Ipilimumab.
REFERENCIAS
1. Martínez Jáñez N. Melanoma. Disponible en http://www.seom.org/es/informacion-sobre-el-cancer/info-tipos- cancer/melanoma (Acceso septiembre 2013).
2. Lin AY, Wang PF, Li H, Kolker JA. Multicohort model for prevalence estimation of advanced malignant melanoma in the USA: an increasing public health concern. Melanoma Res. 2012 Sep 16.
3. Chirlaque MD, Salmerón D, Ardanaz E, Galceran J, Martínez R, Marcos-Gragera R, Sánchez MJ, Mateos A, Torrella A, Capocaccia R, Navarro C. Cancer survival in Spain: estimate for nine major cancers. Ann Oncol. 2010 May;21 Suppl 3:iii21-29.
4. Pollock PM, Meltzer PS: A genome-based strategy uncovers frequent BRAF mutations in melanoma. Cancer Cell 2 (1): 5-7, 2002
5. Ficha Técnica de Zelboraf. Disponible en http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/002409/human_med_001544.jsp&mid=WC0b01ac058001d124 (Acceso septiembre 2013).
6. Assessment Report For Zelboraf (Vemurafenib). Disponible en http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002409/WC500124400.pdf (Acceso septiembre 2013).
7. Chapman PB, Hauschild A, Robert C, Haanen JB, Ascierto P, Larkin J, et al. Improved survival with vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med. 2011 Jun 30;364(26):2507-16.
8. Sosman JA, Kim KB, Schuchter L, Gonzalez R, Pavlick AC, Weber JS, et al. Survival in BRAF V600-mutant advanced melanoma treated with vemurafenib. N Engl J Med. 2012 Feb 23;366(8):707-14.
9. Informe de posicionamiento terapéutico de Yervoy. Agencia Española de Medicamento y Productos Sanitarios. http://www.aemps.gob.es/medicamentosUsoHumano/informesPublicos/docs/IPT-ipilimumab_PT-V1-22022013.pdf. (Acceso septiembre 2013).
10. Flaherty KT, Lee SJ, Zhao F, et al. Phase III Trial of Carboplatin and Paclitaxel With or Without Sorafenib in Metastatic Melanoma. . J Clin Oncol. 2013 Jan 20;31(3):373-9.
11. Hauschild A, Agarwala SS, Trefzer U, Hogg D, Robert C, Hersey P, et al. Results of a phase III, randomized, placebo- controlled study of sorafenib in combination with carboplatin and paclitaxel as second-line treatment in patients with unresectable stage III or stage IV melanoma. J Clin Oncol. 2009 Jun 10;27(17):2823-30.
12. Flaherty KT, Schiller J, Schuchter LM, Liu G, Tuveson DA, Redlinger M, et al. A phase I trial of the oral, multikinase inhibitor sorafenib in combination with carboplatin and paclitaxel. Clin Cancer Res. 2008 Aug 1;14(15):4836-42.
13. Shahabi V, Whitney G, Hamid O, Schmidt H, Chasalow SD, Alaparthy S, Jackson JR. Assessment of association between BRAF- V600E mutation status in melanomas and clinical response to ipilimumab. Cancer Immunol Immunother. 2012 May;61(5):733-7.
14. Assessment Report For Yervoy (ipilimumab). Disponible en http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002213/WC500109302.pdf (Acceso septiembre 2013).
15. Ficha Técnica de Yervoy http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/002213/human_med_001465.jsp&mid=WC0b01ac058001d124. Acceso septiembre 2013.
16. Hodi FS, O'Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen JB, et al. Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med. 2010 Aug 19;363(8):711- 23. Epub 2010 Jun 5. Erratum in: N Engl J Med. 2010 Sep 23;363(13):1290.
17. Dzienis MR, Atkinson V. Response rate to vemurafenib in BRAF-positive melanoma brain metastases. J Clin Oncol 31, 2013 (suppl; abstr 9081).
18. Ribas A, Hodi FS, Callahan M, Konto C, Wolchok J. Hepatotoxicity with combination of vemurafenib and ipilimumab N Engl J Med. 2013 Apr 4;368(14):1365-6.
GRUPO DE EXPERTOS
(por orden alfabético)
Agencia de Evaluación de Tecnologías Sanitarias de Andalucía
Agencia Española de Medicamentos y Productos Sanitarios
Centro de Información Farmacoterapéutica del Servizo Galego de Saúde
Comité de Evaluación de Nuevos Medicamentos en el Ámbito Hospitalario de Euskadi
Programa de Armonización Farmacoterapéutica del Servicio Catalán de la Salud
Los miembros del Consejo asesor y de la Comisión farmacoterapéutica en el ámbito hospitalario pueden consultarse en la página web www.gencat.cat/catsalut.
El Laboratorio Titular, la Sociedad Española de Oncología Médica y el Grupo Español de Pacientes con Cáncer han tenido oportunidad de enviar comentarios al documento, si bien el texto final es el adoptado por el GCPT.
Este protocolo fármaco-clínico ha sido elaborado a petición de la
Comisión Interministerial de Precios.
TABLA DE SUPERVIVENCIA