Informe de Posicionamiento Terapéutico de vandetanib (Caprelsa®) en el cáncer medular de tiroides
INFORME DE POSICIONAMIENTO TERAPÉUTICO PT/V1/15112013.1
Informe de Posicionamiento Terapéutico de Vandetanib (Caprelsa®) en el cáncer medular de tiroides
Fecha de publicación: 22 de noviembre de 2013
El carcinoma de tiroides es el cáncer endocrinológico más frecuente, si bien de manera global sólo representa menos del 1% de todos los cánceres. (1) En España la edad media de aparición del cáncer de tiroides se sitúa entre los 40-53 años, siendo de 2 a 3 veces más frecuente en mujeres que en hombres. En cuanto a datos de incidencia, nuestro país ocupa una posición intermedia entre los países de nuestro entorno, con una tasa de incidencia ajustada por la población europea en 1998 de 2,12 y 5,42 por 100.000 habitantes en varones y mujeres, respectivamente, y una tasa de mortalidad en 2001 de 0,41 y 0,58 por 100.000 habitantes (2).
Histológicamente, el carcinoma de tiroides se suele clasificar en carcinoma diferenciado (CDT), medular y anaplásico. Dentro de los CDT, que representan la inmensa mayoría de los cánceres de tiroides (80-90%), se distinguen el carcinoma papilar y el folicular. Ambos suelen tener buen pronóstico. El cáncer anaplásico es el tipo menos frecuente de los carcinomas de tiroides, pero también el más agresivo y el de peor pronóstico.
El carcinoma medular de tiroides (CMT), el cual representa aproximadamente un 5% de los cánceres de tiroides, se origina a partir de las células parafoliculares C del tiroides, y se caracteriza por la secreción de calcitonina (CTN) y, en menor medida, antígeno carcinoembrionario (CEA). Un 75% de los casos de CMT son esporádicos, mientras que el resto son hereditarios (bien asociado a síndromes de neoplasias endocrinas múltiples tipo MEN2A y MEN2B, o como CMT familiar aislado). Mientras que en la presentación esporádica la edad del diagnóstico suele estar comprendida alrededor de los 60-70 años, la forma hereditaria se suele presentar en pacientes jóvenes y con mutación germinal en el gen RET (Rearranged during Transfection), lo que conlleva la activación de la tirosina-kinasa del RET. Esta mutación del oncogén RET se da en aproximadamente el 30 a 50% de los CMT esporádicos (3,4). La presencia de mutaciones en RET (especialmente si se trata de aquellas en el dominio intracelular, como M918T) se asocia a un peor pronóstico. Recientemente se ha descrito asimismo una elevada frecuencia (entre un 10 y un 40%) de mutaciones somáticas en RAS en CMT esporádicos. Las mutaciones en RET y RAS parecen ser mutuamente excluyentes (5-7)
Para los pacientes con CMT sin evidencia de metástasis a distancia, el tratamiento consiste en la tiroidectomía con extirpación ganglionar cervical, tanto para la forma familiar como la esporádica, con tratamiento sustitutivo con tiroxina. El control de la concentración sérica de calcitonina y de antígeno carcinoembrionario (CEA) es esencial en el seguimiento de este tipo de pacientes (8). En aquellos pacientes con recaídas a nivel local o regional, siempre que sea posible, el tratamiento volverá a ser quirúrgico. Con frecuencia se emplea la radioterapia externa para el control de la enfermedad locorregional en los casos de enfermedad difícilmente resecable. En enfermedad avanzada con metástasis a distancia, la quimioterapia presenta pocas ventajas, con tasas de respuesta menores del 20% y una tasa de supervivencia del 10% a los 10 años. (9-10)
Aunque actualmente existen medicamentos en fases tempranas de investigación clínica (sorafenib y sunitinib), vandetanib es, a fecha de elaboración de este informe, el único medicamento autorizado en la Unión Europea para el tratamiento de este tumor.
VANDETANIB (CAPRELSA®)
Caprelsa está indicado para el tratamiento del cáncer medular de tiroides agresivo y sintomático en pacientes con enfermedad no resecable localmente avanzada o metastásica (11).
Caprelsa se presenta como comprimidos recubiertos con película de 100 y 300 mg de vandetanib.
La dosis recomendada es 300 mg una vez al día, tomada con o sin alimentos, aproximadamente a la misma hora cada día. Vandetanib puede administrarse hasta que los pacientes con CMT no se beneficien más del tratamiento.
Este medicamento tiene una autorización de comercialización condicional, lo que significa que se aportarán más pruebas en relación al mismo, en particular, en lo que respecta a la magnitud del beneficio en pacientes sin la mutación RET. Cada año, la Agencia Europea de Medicamentos (EMA) revisará la nueva información disponible (11-12).
Farmacología
Vandetanib es un potente inhibidor de las tirosinas quinasas del receptor-2 del factor de crecimiento endotelial vascular (VEGFR-2, también conocido como receptor con dominio de inserción de quinasa [KDR]), del receptor del factor de crecimiento epidérmico (EGFR) y del RET. Vandetanib es también un inhibidor submicromolar de la tirosina quinasa del receptor-3 del endotelio vascular (VEGFR3).
In vivo, la administración de vandetanib reduce la angiogénesis inducida por células tumorales, la permeabilidad de los vasos del tumor y la densidad de los microvasos del tumor, e inhibe el crecimiento tumoral de un rango de modelos de xenoinjertos tumorales humanos en ratones atímicos. Vandetanib también inhibe el crecimiento de xenoinjertos tumorales del CMT in vivo.
Sin embargo, se desconoce el mecanismo de acción preciso de vandetanib en el CMT localmente avanzado o metastásico.
La documentación de farmacocinética consistió en 16 estudios fase I, 3 estudios fase II y 3 estudios fase III. (12) Tras la administración oral de vandetanib, la absorción es lenta y las concentraciones plasmáticas máximas se alcanzan generalmente a una mediana de 6 horas, con un rango de 4-10 horas, después de dicha administración. El estado estacionario se alcanza a partir de aproximadamente 2 meses. Vandetanib tiene una unión a proteínas plasmáticas in vitro de aproximadamente el 90%. La farmacocinética de vandetanib a la dosis de 300 mg en pacientes con CMT se caracteriza por un volumen de distribución de aproximadamente 7.450 litros, con un aclaramiento de aproximadamente 13,2 litros/hora y una semivida plasmática de aproximadamente 19 días. La exposición a vandetanib no está afectada por los alimentos.
Eficacia
La eficacia clínica está basada en un ensayo pivotal (estudio 58) y dos estudios fase II no controlados llevados a cabo con dosis de 100 y 300 mg (12).
El ensayo pivotal fue un estudio aleatorizado, doble ciego, controlado con placebo para demostrar la seguridad y eficacia de vandetanib 300 mg. (12,13) Este estudio incluyó 331 pacientes con CMT no resecable localmente avanzado o metastásico, tanto hereditario como esporádico. Los pacientes debían tener una expectativa de vida superior a las 12 semanas con un estado funcional OMS 0-2 (criterio de la Organización Mundial de la Salud). Se excluyeron aquellos sujetos con metástasis cerebrales o compresión medular, a no ser que estuvieran tratados desde 4 semanas antes de la primera dosis y con un tratamiento estable sin esteroides durante al menos 10 días. Sólo se incluyeron pacientes con calcitonina (CTN) ≥ 500 pg/ml (unidades convencionales) o ≥ 146,3 pmol/l (unidades internacionales estándar).
Los pacientes recibieron 300 mg al día de vandetanib o placebo hasta la progresión de la enfermedad. En el momento de la progresión, se interrumpió el tratamiento ciego del estudio y los pacientes tuvieron la opción de recibir vandetanib de manera abierta.
El objetivo principal de este estudio fue demostrar una mejoría en la supervivencia libre de progresión (SLP, definida como tiempo desde la aleatorización hasta la progresión objetiva del tumor o muerte por cualquier causa con vandetanib comparado con placebo). Las variables secundarias fueron evaluación de la tasa de respuesta objetiva global (TRO), tasa de control de la enfermedad (TCE), definida como respuesta parcial (RP) o respuesta completa o enfermedad estable que dure al menos 24 semanas, duración de la respuesta, tiempo hasta el empeoramiento del dolor y supervivencia global (SG). La variable principal SLP, la TRO y la TCE se basaron en la revisión ciega independiente y centralizada de las pruebas de imagen de acuerdo a criterios RECIST modificados.
El análisis principal fue predefinido en la población por intención de tratar (ITT).
El estudio fue llevado a cabo en 63 centros internacionales, reclutando a 437 pacientes de los que 331 sujetos fueron aleatorizados con una ratio de 2:1. Un 57.4% de los pacientes fueron hombres y un 95.2% caucásicos. El 81% había recibido radioterapia previa y un 20.5 % quimioterapia. A nivel basal, hubo menos pacientes con enfermedad estable en el grupo activo y más con progresión de la enfermedad (6.1 % vs. 11.0 % y 7.8 % vs. 1.0%)(*). La mayoría de los pacientes presentaba al inicio un estado funcional de 0-1 con CMT esporádico (>85%) y un estadio M1 (94.6%).
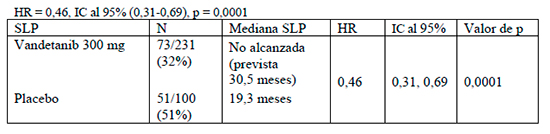
No se pudo calcular la mediana de SLP, ya que se había producido un número insuficiente de eventos en el momento del análisis. Se realizó una estimación de la SLP de vandetanib mediante un modelo de Weibull. La mediana de SLP de vandetanib fue de 30,5 meses vs. 19,3 meses del grupo placebo (HR: 0,46; IC95%: 0,31-0,69, p <0,0001).
La superioridad de vandetanib sobre placebo fue consistente en todos los análisis de subgrupos preespecificados.
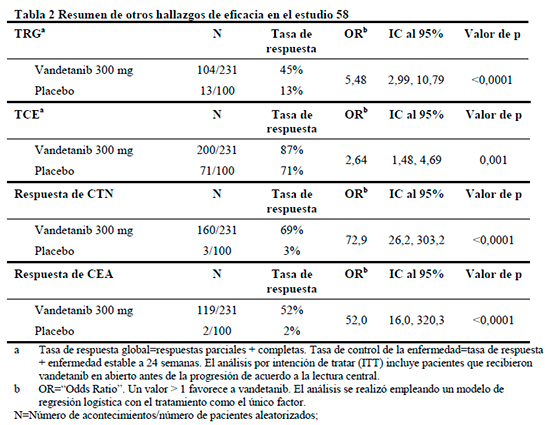
Los resultados de las variables secundarias, TRO global [45 % vs. 13.0 %, OR 5.48 IC 95% (2.99, 10.79)] y TCE [OR 2.64 IC 95% (1.48, 4.69)], apoyaron el beneficio mostrado en la variable primaria. 12 de las 13 respuestas observadas (respuestas completas o respuestas parciales según criterios RECIST) en los pacientes inicialmente aleatorizados a placebo ocurrieron mientras recibían vandetanib en la fase abierta (12, 13).
Sin embargo, no hubo diferencias estadísticamente significativas en supervivencia global [HR 0.89 IC 95% (0.28, 2.85)]. Estos datos son inmaduros y su interpretación podría estar limitada por el escaso número de eventos (14% de fallecimientos en el grupo de vandetanib y 16% en el grupo de placebo) en el momento del análisis y por el elevado número de pacientes en el brazo placebo (58%) que recibieron vandetanib en la fase abierta tras evidenciarse progresión de la enfermedad.
Aquellos pacientes que a nivel basal presentaron una duplicación de la concentración (DT) de CEA y CTN en un tiempo menor de 24 meses, obtuvieron mayores tasas de respuesta respecto a los sujetos en los que la DT tanto en CEA como en CTN fue mayor de 24 meses (53.6% versus 37 % para CEA y 46.8% vs. 39.8 % para CTN). Los pacientes con una mayor masa tumoral a nivel basal, obtuvieron mayor beneficio en términos de SLP (42.1% vs. 63.6% y 21.4% vs. 35.6%; expresado en % de pacientes con progresión en el grupo de vandetanib vs. placebo para pacientes con mayor masa tumoral respecto a pacientes con menor masa tumoral).
La mutación RET fue positiva en 187 (56.5%) pacientes, desconocida en 138 (41.1%) y negativa en 8 (2.4%) sujetos. A los 12 meses, la tasa de progresión (vandetanib vs. placebo) fue del 34.3 % (47/137) vs. 54.0 % (27/50) en sujetos RET positivo, 27.2 % (25/92) vs. 43.2 % (19/44) en pacientes con RET desconocido y un 50.0 % (1/2) vs. 83.3 % (5/6) en sujetos con RET negativo.
En un análisis posterior de 79 pacientes con ausencia de mutaciones en RET, de los que 46 habían sido aleatorizados a vandetanib y 33 a placebo, la tasa de respuesta global para vandetanib fue de 35% (vs. 52% en los 187 pacientes con mutación RET positiva). Respecto al beneficio en SLP frente a placebo los resultados no fueron estadísticamente significativos en pacientes con mutación RET negativa (HR de 0,57 [IC 95% 0,29-1,13]).
Finalmente, hubo una mejora en el tiempo hasta el empeoramiento del dolor en el grupo en tratamiento con vandetanib comparado con placebo (HR: 0,61 [IC 95%: 0,43-0,87]). La mediana de tiempo hasta el empeoramiento del dolor fue de 7,85 meses vs. 3,25 meses del brazo placebo.
Seguridad
Un total de aproximadamente 4.000 pacientes han sido expuestos a vandetanib.
En el estudio pivotal, la duración media de exposición al tratamiento con vandetanib fue de aproximadamente 74 semanas con una mediana de 90.1 semanas. 162 pacientes fueron tratados con vandetanib durante al menos 12 meses y 51 sujetos durante al menos 24 meses. Un total de 49.4% de los pacientes tratados con vandetanib experimentaron alguna reducción o interrupción de dosis (un 35.1 % de pacientes fueron tratados con 200 mg por problemas de tolerabilidad) y un 12% tuvo que interrumpir de forma definitiva el fármaco por toxicidad.
Los cinco efectos adversos (EA) recogidos más frecuentemente en el estudio principal dentro del grupo de vandetanib fueron diarrea, rash, nausea, hipertensión y cefalea.. El porcentaje de pacientes con grado 3 o mayor de EA fue 2,3 veces mayor en el grupo tratado con vandetanib frente al tratado con placebo (55.4% vs. 24.2%). [Diarrea (11%); hipertensión (9%), prolongación del intervalo QTc (8%), fatiga (6%), disminución del apetito (4%) y rash (4%)].
El porcentaje de pacientes con al menos un efecto adverso grave (EAG) fue más alto en el grupo tratado con el fármaco experimental (30.7% vs. 13.1%). Los EAG más frecuentes fueron diarrea (2.2%), neumonía (2.2%), disminución del apetito (1.7%), crisis hipertensivas (1.7%), infección del tracto urinario (1.3%), dolor abdominal (1.3%) hipercalcemia (1.3%), hipertensión (1.3%) y bronquitis (0.9%).
En la población total de estudio, un 13.9% de las muertes se dieron en pacientes tratados con vandetanib frente a un 15.2 % de pacientes tratados con placebo. Siete pacientes tuvieron un AE con resultado de muerte, 5 en el brazo de vandetanib y 2 en el de placebo.(12, 13).
Las reacciones adversas más frecuentes con vandetanib comunicadas en los ensayos clínicos, incluyen, nasofaringitis, bronquitis, infecciones del tracto respiratorio superior, infecciones del tracto urinario, disminución del apetito, hipocalcemia, insomnio, depresión, cefalea, parestesia, disestesia, mareo, visión borrosa, cambio estructural de la córnea, prolongación del intervalo QTc del ECG, hipertensión, dolor abdominal, diarrea, náusea, vómitos, dispepsia, reacciones de fotosensibilidad, rash, proteinuria, nefrolitiasis, astenia, fatiga, dolor y edema.
Con respecto a los efectos pro-arritmogénicos de vandetanib, su administración a una dosis de 300 mg se asocia a una prolongación sustancial en el QTc (8%) dependiente de la concentración. A este respecto la ficha técnica del medicamento recoge de manera clara advertencias y contraindicaciones en pacientes de riesgo.
Otros efectos adversos de interés, descritos en los ensayos con vandetanib han sido la nefrotoxicidad, la neurotoxicidad periférica y la leucoencefalopatía posterior reversible (12).
Se ha sugerido que los pacientes con una escasa masa muscular podrían estar expuestos a niveles superiores del fármaco y presentar por tanto una mayor toxicidad (14).
DISCUSIÓN
El efecto de vandetanib sobre los pacientes con CMT con enfermedad no resecable localmente avanzada o metastásica es, en términos de supervivencia libre de progresión, clínicamente relevante. No obstante, el objetivo de todo tratamiento oncológico incapaz de alcanzar la curación del tumor, es incrementar la supervivencia global junto con la calidad de vida del paciente. Debido al bajo número de muertes registradas en el estudio principal de vandetanib es poco probable que se alcanzara el objetivo de aumentar la supervivencia global, sobre todo debido a la relativa “alta supervivencia a corto plazo (1-2 años)” de estos pacientes y al factor de confusión que se crea tras el cruce de los pacientes tratados con placebo a vandetanib tras la progresión de la enfermedad. En principio, podría esperarse que un mayor tiempo de supervivencia libre de progresión se acompañe de una disminución en los síntomas asociados a la progresión del tumor.
Si bien el estudio señala una mejoría en el tiempo hasta el empeoramiento del dolor basado en la escala para medir la intensidad de dolor BPI [7.85 meses vs. 3.25 meses (HR 0.61, 95% CI 0.43, 0.87)], no se ha demostrado mejoría significativa en otros síntomas relacionados directamente con el tumor o en la calidad de vida global del paciente. Por tanto, el perfil de seguridad puede, de una manera indirecta, indicar hasta qué punto el tratamiento con vandetanib en pacientes con CMT aumenta no sólo el tiempo hasta la progresión, sino en qué condiciones para el paciente. Ciertamente, el perfil de seguridad muestra una alta frecuencia de efectos adversos, disminuciones y en menor medida interrupciones de dosis debidas a la mala tolerabilidad del fármaco y a efectos graves a nivel cardiaco y renal. Por tanto, aunque el medicamento demuestra un efecto antitumoral clínicamente relevante retrasando la progresión de la enfermedad, dada su alta toxicidad, y ante la ausencia de efectos en la calidad de vida del paciente y de incremento en la supervivencia, parece lógico limitar su uso a los pacientes que puedan obtener el mayor beneficio a expensas de su mala tolerabilidad.
La mediana de SLP en el grupo placebo fue de 19.3 meses, lo que podría indicar que muchos pacientes reclutados en el estudio no estaban realmente en progresión clara de la enfermedad, ya que de otra forma el tiempo hasta la progresión hubiese sido significativamente menor en el grupo control.
Otro aspecto importante es la posible menor actividad en los pacientes con mutación RET negativa. Cierto es que en el subgrupo de pacientes con estatus desconocido para RET la eficacia parece ser menor. No obstante, los resultados en tasa de progresión (vandetanib vs. placebo) a los 12 meses no parecen estar resaltando una ausencia de eficacia, sino más bien una incertidumbre en la magnitud de la misma.
En relación al análisis a posteriori en el grupo con ausencia de mutación en RET, los datos señalan una tendencia positiva en términos de SLP (HR =0,57 IC95% 0,29-1,13) si bien, no es estadísticamente significativa, aunque probablemente por el tamaño de la muestra. Sin embargo, en la identificación de estos pacientes, en 71 de ellos, la secuenciación de los 6 exones fue incompleta y algunos pacientes con resultado RET negativo para mutación M918T podrían ser positivos para mutación de otros exones.
En base a estos datos, limitar el uso a pacientes con la mutación positiva, no parece a priori recomendable dada la ausencia concluyente de datos y la incertidumbre sobre el grado de eficacia en estos pacientes, si bien, futuros estudios podrían arrojar más luz a este respecto.
En este sentido y de acuerdo a la ficha técnica del medicamento, en el caso de pacientes en los que la mutación del oncogén RET no se conoce o es negativa, antes de la decisión individual de tratamiento se debe tener en cuenta la posibilidad de un menor beneficio. Así y a pesar de que la evidencia disponible no es totalmente concluyente, se recomienda el estudio de la presencia de mutaciones en RET (y en los casos negativos, también en RAS) en los tumores de los pacientes con CMT esporádico candidatos a tratamiento con vandetanib.
En relación a la seguridad, no es posible establecer recomendaciones claras sobre posibles reducciones de la dosis de 300mg salvo las establecidas en Ficha Técnica para poblaciones especiales (11). En este sentido, el estudio 68, fase II con dosis de 100 mg, mostró tasas de respuesta del 15,8% y duraciones de respuesta de 5,5 meses, inferiores a los reportados con dosis de 300 mg (16). Están pendientes los resultados de un estudio en el que la dosis de 150 mg es comparada con la de 300 mg.
En cuanto a los parámetros que pueden indicar qué subpoblaciones podrían obtener un mejor balance del beneficio- riesgo, merece la pena mencionar los subgrupos de pacientes en base a los niveles basales del antígeno carcinoembrionario (CEA), calcitonina (CTN), tamaño del tumor y sintomatología. Tanto el CEA como la CTN son dos indicadores de la progresión del tumor. Así, la velocidad con la que las concentraciones de CTN y CEA se duplican (DT), pueden ayudar a identificar los pacientes con un peor pronóstico. Los pacientes con DT en CEA y CTN menores de 24 meses, obtuvieron mayores tasas de respuesta respecto a los sujetos en los que la DT tanto en CEA como en CTN fue mayor de 24 meses (53.6% versus 37 % para CEA y 46.8% vs. 39.8 % para CTN).
El tamaño de la masa tumoral también parece jugar un papel en la respuesta obtenida. Si bien el beneficio en términos de SLP fue demostrado tanto para los pacientes con tumores por encima como por debajo de los 10 cm, los datos existentes parecen indicar que la eficacia podría ser mayor en aquellos sujetos con tumores mayores de 10 cm antes del tratamiento.
En relación a la sintomatología de los pacientes antes de empezar el tratamiento (diarrea, fatiga, dolor, síntomas respiratorios, pérdida de peso, disfagia), el análisis según porcentaje de pacientes en progresión objetiva del tumor, muestra una tendencia a que los pacientes “asintomáticos” obtendrían un menor beneficio frente aquellos claramente sintomáticos (36.1% en el brazo de vandetanib vs. 59.2% en el brazo de placebo en pacientes sintomáticos a nivel basal y 22.4% vs. 31% para pacientes asintomáticos a nivel basal para vandetanib y placebo respectivamente) (*).
Por último, el 95% de los pacientes aleatorizados en el estudio pivotal tuvieron metástasis a nivel basal. Únicamente 14 de los pacientes tratados no tenían metástasis, por lo que el beneficio clínico del tratamiento con vandetanib en pacientes con únicamente enfermedad locorregional no controlada debería ser considerado en base a la presencia o no de sintomatología y tras cirugía y/o radioterapia si procede.
CONCLUSIÓN
Vandetanib, si bien ha mostrado un retraso en la progresión del tumor, no ha demostrado que proporcione un beneficio claro para el paciente en términos de supervivencia global o mejora en la calidad de vida. Este hecho, unido a su perfil de seguridad limitan la población donde el balance beneficio riesgo puede a priori considerarse positivo. Así, el redactado de la indicación específica que únicamente aquellos pacientes con cáncer medular de tiroides agresivo y sintomático podrán beneficiarse del tratamiento con vandetanib.
Por tanto, teniendo en cuenta los datos disponibles y la falta de alternativas terapéuticas, parece razonable recomendar el empleo de vandetanib en:
- Pacientes con cáncer medular de tiroides agresivo y sintomático con enfermedad metastásica, en los que exista evidencia radiológica de una franca progresión tumoral, así como una clara sintomatología clínica asociada a la enfermedad.
- Pacientes con cáncer medular de tiroides agresivo y sintomático con enfermedad metastásica, en los que las lesiones no sean evaluables radiológicamente y que presenten un tiempo de duplicación de CTN o CEA menor de 24 meses.
- Pacientes con enfermedad locorregional no controlada y claramente sintomática, tras cirugía y/o tratamiento con radioterapia (incluso en ausencia de metástasis).
Por último, recomendamos el estudio de la presencia de mutaciones en RET (y en los casos negativos, también en RAS) en los tumores de los pacientes con CMT esporádico candidatos a tratamiento con vandetanib.
REFERENCIAS
1. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines)®. Thyroid Carcinoma. Versión 2.2013 (acceso Julio 2013).
2. Asociación Española de Cáncer de Tiroides (AECAT) www.aecat.net.
3 Uchino S, Noguchi S, Yamashita H, Sato M, Adachi M, Yamashita H, Watanabe S, Ohshima A, Mitsuyama S, Iwashita T, Takahashi M. Somatic mutations in RET exons 12 and 15 in sporadic medullary thyroid carcinomas: different spectrum of mutations in sporadic type from hereditary type. Jpn J Cancer Res 1999 Nov;90(11):1231-7.
4 Eng C, Smith DP, Mulligan LM, Nagai MA, Healey CS, Ponder MA, Gardner E, Scheumann GF, Jackson CE, Tunnacliffe A, et al. Point mutation within the tyrosine kinase domain of the RET proto- oncogene in multiple endocrine neoplasia type 2B and related sporadic tumours. Hum. Mol. Genet. 1994 Feb;3(2):237-41.
5. Moura MM, Cavaco BM, Pinto AE, Leite V.et al High prevalence of RAS mutations in RET-negative sporadic medullary thyroid carcinomas. J Clin Endocrinol Metab 2011 May;96(5): E863-8.
6. Ciampi R, Mian C, Fugazzola L, Cosci B, Romei C, Barollo S, Cirello V, Bottici V, Marconcini G, Rosa PM, Borrello MG, Basolo F, Ugolini C, Materazzi G, Pinchera A, Elisei R. Evidence of a low prevalence of RAS mutations in a large medullary thyroid cancer series. Thyroid. 2013 Jan;23(1):50-7.
7. Agrawal N, Jiao Y, Sausen M, Leary R, Bettegowda C, Roberts NJ, Bhan S, Ho AS, Khan Z, Bishop J, Westra WH, Wood LD, Hruban RH, Tufano RP, Robinson B, Dralle H, Toledo SP, Toledo RA, Morris LG, Ghossein RA, Fagin JA, Chan TA, Velculescu VE, Vogelstein B, Kinzler KW, Papadopoulos N, Nelkin BD, Ball DW. Exomic sequencing of medullary thyroid cancer reveals dominant and mutually exclusive oncogenic mutations in RET and RAS. J Clin Endocrinol Metab. 2013 Feb;98(2):E364-9.
8. Elisei R, Bottici V, Luchetti F, Di Coscio G, Romei C, Grasso L, et al. Impact of routine measurement of serum calcitonin on the diagnosis and outcome of medullary thyroid cancer: experience in 10,864 patients with nodular thyroid disorders. J Clin Endocrinol Metab 2004;89:163–8.
9. Pacini F., Castagna M. G, Brilli L & Pentheroudakis G. Thyroid cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 23 (Supplement 7): vii110– vii119, 2012.
10. Schlumberger M, Bastholt L, Dralle H, Jarzab B, Pacini F, Smit JWA. 2012 European Thyroid Association Guidelines for Metastatic Medullary Thyroid Cancer. Eur Thyroid J. 2012;1:5–14.
11. Ficha técnica de Caprelsa (vandetanib). Disponible en http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002315/WC500123555.pdf. (Acceso Julio 2013).
12. Assessment Report for Caprelsa (vandetanib). Disponible en http://www.ema.europa.eu/docs/en_GB/document_library/Summary_of_opinion_-_Initial_authorisation/human/002315/WC500117817.pdf (Acceso Julio 2013).
13. Wells SA Jr, Robinson BG, Gagel RF, et al: Vandetanib in patients with locally advanced or metastatic medullary thyroid cancer: A randomized, double blind phase III trial. J Clin Oncol doi: 10.1200/JCO.2011.35.5040.
14. Massicotte MH, Borget I, Broutin S, Baracos VE, Leboulleux S, Baudin E, Paci A, Deroussent A, Schlumberger M, Antoun S. Body composition variation and impact of low skeletal muscle mass in patients with advanced medullary thyroid carcinoma treated with vandetanib: results from a placebo-controlled study J Clin Endocrinol Metab. 2013 Mar 29.
15. Schoffski P, Elisei R, Muller S, Brose MS, Shah MH, Licitra LF, et al. An international, double-blind, randomized, placebo-controlled phase III trial (EXAM) of cabozantinib (XL184) in medullary thyroid carcinoma (MTC) patients (pts) with documented RECIST progression at baseline. J Clin Oncol 2012;30(15):5508.
16. Robinson BG, Paz-Ares L, Krebs A, Vasselli J, Haddad R. Vandetanib (100 mg) in patients with locally advanced or metastatic hereditary medullary thyroid cancer. J Clin Endocrinol Metab 2010;95:2664-71. (*)No se ha incluido información de carácter comercial-confidencial.
GRUPO DE EXPERTOS
(por orden alfabético)
Agencia de Evaluación de Tecnologías Sanitarias de Andalucía
Javier Aller
Facultativo Especialista Adjunto del Servicio de Endocrinología. Hospital Universitario Puerta de Hierro Majadahonda. Madrid.
Jorge Camarero Jiménez.
División de Farmacología y Evaluación Clínica. Agencia Española de Medicamentos y Productos Sanitarios. Madrid.
Concepción Prieto Yerro.
Comité de Medicamentos de Uso Humano (CHMP) de la EMA. Unidad CHMP de la Agencia Española de Medicamentos y Productos Sanitarios. Madrid.
Programa de Armonización Farmacoterapéutica del Servicio
Catalán de la Salud
Los miembros del Consejo asesor y de la Comisión farmacoterapéutica en el ámbito hospitalario pueden consultarse en la página web www.gencat.cat/catsalut .
Arantxa Sancho López.
Comité de Medicamentos de Uso Humano (CHMP) de la EMA. Servicio de Farmacología Clínica. Hospital Universitario Puerta de Hierro. Majadahonda. Madrid.
María Luisa Suárez Gea.
Jefe de División de Farmacología y Evaluación Clínica. Agencia Española de Medicamentos y Productos Sanitarios. Madrid.
Elisa Sulleiro Avendaño
Unidad CHMP de la Agencia Española de Medicamentos y Productos Sanitarios. Madrid.
La Asociación Española de Cáncer de Tiroides (AECAT) y el laboratorio Titular de la Autorización de Comercialización del medicamento también han proporcionado comentarios a este informe.
Este protocolo fármaco-clínico ha sido elaborado a petición de la Comisión Interministerial de Precios.