Informe de Posicionamiento Terapéutico de regorafenib (Stivarga®) en tumores del estroma gastrointestinal (GIST)
INFORME DE POSICIONAMIENTO TERAPÉUTICO PT-REGORAFENIB-GIST/V1/10042015
Informe de Posicionamiento Terapéutico de regorafenib (Stivarga®) en tumores del estroma gastrointestinal (GIST)
Fecha de publicación: 10 de abril de 2015
El tumor del estroma gastrointestinal (GIST por sus siglas en inglés) es un grupo de tumores mesenquimales que se engloba dentro de los sarcomas viscerales. Representan el 2% de los tumores digestivos, siendo su localización variable, aunque con cierta preferencia por la localización gástrica (60%) (1). La incidencia en nuestro país se estima en 1,11-1,24 casos por 100.000 hab/año (2,3), la cual es bastante similar a incidencia a nivel europeo (4).
El tratamiento de primera elección del GIST es la cirugía, siempre y cuando el tumor sea resecable y no exista evidencia de enfermedad metastásica. La resección completa del tumor es potencialmente curativa. Sin embargo, aproximadamente el 40% de estos pacientes progresan a enfermedad metastásica (5). En pacientes con presencia de metástasis o en aquellos con GIST no resecable, el tratamiento farmacológico basado en dianas moleculares es aceptado hoy en día como terapia de elección. Sobre un 95% de los GISTs expresan el antígeno CD117, un antígeno basado en el receptor KIT de tirosin kinasa (6). Actualmente, imatinib y sunitinib tienen la indicación para el tratamiento del GIST, y se consideran tratamientos de referencia en GIST (7).
Imatinib está autorizado en el tratamiento de pacientes adultos con GISTs malignos no resecables y /o metastásicos Kit (CD117) positivos, y en el tratamiento adyuvante de pacientes adultos que presentan un riesgo significativo de recaí da después de la resección de GIST Kit (CD117) positivo. Los pacientes que tienen un riesgo bajo o muy bajo de recaída no deben recibir tratamiento adyuvante. La variable principal de eficacia en los ensayos de enfermedad avanzada fue la tasa de respuesta objetiva, mientras que en los de adyuvancia fue supervivencia libre de recidiva.
Sunitinib está autorizado en el tratamiento de GISTs no resecables y /o metastásicos en adultos después del fracaso al tratamiento con imatinib debido a resistencia o intolerancia. La variable principal de eficacia fue el tiempo hasta la progresión tumoral.
REGORAFENIB (STIVARGA®)
Regorafenib está autorizado para el tratamiento de GISTs irresecables o metastásicos en pacientes que progresaron durante el tratamiento previo con imatinib y sunitinib o son intolerantes al mismo (8).
La dosis recomendada de regorafenib es 160 mg (4 comprimidos de 40 mg), administrados una vez al día durante 3 semanas seguidas de 1 semana sin tratamiento. Este período de 4 semanas se considera un ciclo de tratamiento.
Farmacología
Regorafenib es un fármaco antitumoral oral que bloquea varias proteinquinasas, incluidas las quinasas implicadas en la angiogénesis tumoral (VEGFR1, -2, -3, TIE2), la oncogénesis (KIT, RET, RAF-1, BRAF, BRAFV600E) y el microambiente tumoral (PDGFR, FGFR) (9). En concreto inhibe el KIT mutado, un importante controlador oncogénico en los tumores del estroma gastrointestinal, y por lo tanto, bloquea la proliferación celular tumoral.
Eficacia
El estudio 14874 (GRID) es un ensayo clínico fase III multicéntrico, aleatorizado (2:1), doble ciego y comparado con placebo en pacientes con GIST irresecable y/o metastásico previamente tratados con al menos dos inhibidores de la tirosina kinasa (imatinib y sunitinib) (6,10).
Todos los pacientes incluidos en el estudio pivotal fueron adultos que habían progresado a pesar del tratamiento con imatinib (o que hubieran presentado intolerancia al mismo) y que hubieran progresado también durante el tratamiento con sunitinib. También se permitió el reclutamiento de pacientes que hubieran progresado a otros tratamientos salvo en caso de que éste hubiera sido con otros inhibidores VEGFR. El estado de ECOG-Performance Status de los pacientes fue de 0-1. Se excluyeron del estudio pacientes con metástasis cerebrales sintomáticas o los tumores meníngeos, además de los feocromocitomas, hipertensión no controlada, angina de pecho inestable, infarto de miocardio en los 6 meses anteriores, insuficiencia cardiaca clase 2 (NYHA), arritmias que requiriesen tratamiento farmacológico (excepto beta bloqueantes y digoxina) eventos trombóticos venosos en los 3 meses previos, fenómenos hemorrágicos > grado 3 y proteinuria persistente.
El estudio incluyó 199 pacientes, de los cuales 133 recibieron regorafenib y los restantes placebo, vía oral durante tres semanas (con una semana adicional sin tratamiento). En los dos brazos, los pacientes recibieron además el mejor tratamiento de soporte en función de la sintomatología presentada.
El objetivo principal del estudio fue demostrar la superioridad de regorafenib frente a placebo en la supervivencia libre de progresión (SLP) evaluada por el comité independiente. Se incluyeron como variables secundarias supervivencia global (SG), tiempo hasta progresión y tasa de respuesta objetiva (TRO) entre otras. Se incluyeron como variables exploratorias calidad de vida relacionada con la salud (cuestionarios EORTC QLQ C30 y EQ5D)
El análisis de SLP se realizó tras observarse 144 acontecimientos, obteniéndose un HR=0,27 (IC95% 0,18-0,4) y una mediana de la SLP de 4,8 meses frente a 0,9 meses, resultado estadísticamente significativo (Tabla 1 y Figura 1).
Tabla 1: SLP tras 144 eventos (estudio GRID)
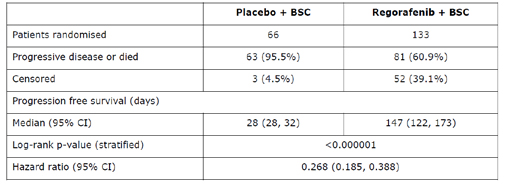
Los resultados fueron consistentes en los diferentes análisis de subgrupos (incluyendo criterios de estratificación: tercera línea frente a cuarta línea o sucesivas de tratamiento y región geográfica: Asia frente el resto del mundo) excepto en el subgrupo de pacientes en los que la duración del tratamiento con imatinib fue menor a 6 meses.
En relación con las variables secundarias, no se observaron diferencias estadísticamente significativas en cuanto a SG entre ambos grupos: HR=0,772 (IC95% 0,423-1,408).
Figura 1: Curva de supervivencia libre de progresión (Kaplan-Meier)
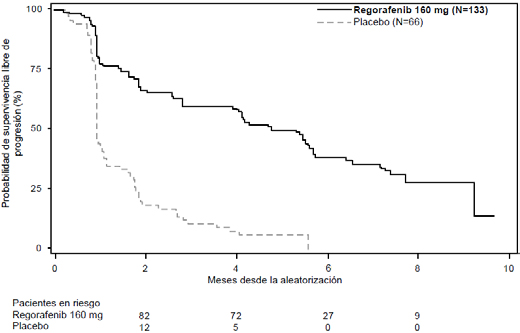
Ninguno de los brazos alcanzó la mediana de SG. En el momento del análisis, el 84% de los pacientes (56/66) del brazo placebo habían cruzado al brazo de regorafenib en régimen abierto tras detectarse progresión de la enfermedad. En un análisis posterior actualizado con 139 eventos, se mantuvo la no significación estadística, con un HR= 0,85 (IC95% 0,6-1,2). Tampoco hubo diferencias estadísticamente significativas en la TRO, aunque sí se observaron en la variable de tiempo hasta progresión, con un HR=0,25 (IC95% 0,17-0,36) y una mediana de 5,4 meses en el grupo de regorafenib frente a 0,9 meses en el grupo de placebo (Tabla 2 y Figura 2).
Tabla 2: resultados de eficacia del estudio GRID
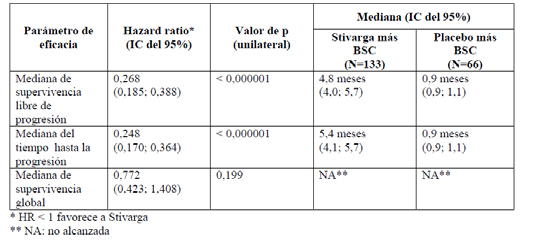
Respecto a las variables relacionadas con calidad de vida, de manera general y con las limitaciones del análisis exploratorio, se observó cierto deterioro en los pacientes tratados con regorafenib frente a placebo.
Cincuenta y seis pacientes del grupo placebo cruzaron al grupo de regorafenib y cuarenta y un pacientes tratados con regorafenib continuaron el tratamiento tras la progresión de la enfermedad. La mediana de la SLP secundaria (medida por el investigador) fue de 5,0 y 4,5 meses, respectivamente.
También fueron comunes reacciones adversas como la hipertensión (59,1% frente a 27,3%), diarrea (37,9% frente a 9,1%), fatiga (37,1% frente a 28,8%), disminución del apetito (31,1% frente a 21,2%), estreñimiento (28% frente a 22,7%) y rash (25,8% frente a 3,0%).
Seguridad
Las reacciones adversas más comunes en el estudio GRID fueron de reacción cutánea mano-pie (65,9% en los pacientes tratados con regorafenib, frente al 15,2% en los que recibieron placebo), apareciendo durante el primer ciclo de tratamiento y en un 44,7% de los casos con intensidad leve a moderada.
Figura 2. Curva de supervivencia global (Kaplan-Meier)

La mayoría de casos de hipertensión durante el tratamiento con regorafenib se produjeron durante el primer ciclo de tratamiento y en un 31,1% de los casos fueron de intensidad leve a moderada.
En todos los ensayos clínicos, los acontecimientos correspondientes a trastornos cardiacos (de todos los grados) se notificaron con mayor frecuencia (20,5% frente a 10,4%) en los pacientes tratados con regorafenib de edad igual o superior a 75 años (N=78) que en los pacientes tratados con regorafenib de edad inferior a 75 años (N=995).
Los pacientes tratados con regorafenib presentaron una incidencia mayor de efectos adversos grado 3 en comparación con los tratados con placebo (64,4% frente a 25,8%). El 62,9% de los pacientes tratados con regorafenib sufrieron efectos adversos que condujeron a la modificación de la dosis frente al 9,1% en el grupo placebo.
Las reacciones adversas más graves en los pacientes tratados con regorafenib son lesión hepática grave, hemorragia y perforación gastrointestinal. Se produjo lesión hepática inducida por fármacos (LHIF) grave con desenlace fatal en 3 pacientes de más de 1.200 pacientes tratados con regorafenib en todos los ensayos clínicos (0,25%).
Hubo 7 pacientes en el brazo de regorafenib (5,3%) y 3 en el brazo de placebo (4,5%) que fallecieron durante el tratamiento o en los 30 primeros días tras el cese definitivo de tratamiento.
Se deberá valorar individualmente la necesidad de reducir la dosis de regorafenib o interrumpir temporalmente la medicación (o permanentemente en los casos graves o persistentes) en caso de aparición de algunos de estos efectos adversos (5).
La incidencia de reacciones adversas que dieron lugar a descontinuación del tratamiento en el estudio GRID fue de 8 pacientes (6,1%) en el brazo de regorafenib frente a 5 pacientes (7,6%) en el brazo de placebo.
El perfil de seguridad de regorafenib parece en definitiva común a otras moléculas implicadas en la angiogénesis tumoral e inhibidores de tirosin kinasas. Hipertensión, síndrome mano-pie, rash, diarrea, mucositis y toxicidad hematológica.
DISCUSIÓN
El tratamiento con regorafenib ha mostrado un aumento significativo y clínicamente relevante en la SLP respecto al uso de placebo en una población con escasas alternativas terapéuticas y cuyos tratamientos previos habían sido agotados. Este beneficio en términos de SLP se traduce en una ganancia de aproximadamente unos 4 meses. El resultado puede considerarse robusto teniendo en cuenta los subgrupos analizados y análisis posteriores de sensibilidad, salvo en el grupo en el que la duración del tratamiento con imatinib fue inferior a 6 meses, aunque dado lo limitado de la muestra (n=20) y el amplio intervalo de confianza debe interpretarse con precaución.
El retraso en la progresión tumoral se debe fundamentalmente a los casos en los que el tratamiento con regorafenib consiguió una estabilización de la enfermedad, ya que la TRO fue reducida (TRO 4,1% vs. 1,5% regorafenib y placebo respectivamente). No hubo respuestas completas en ninguno de los dos grupos.
El beneficio mostrado en SLP no se traduce, de acuerdo a los datos del estudio, en una mejora de la supervivencia (ambos grupos presentaron una mediana de supervivencia de 17,4 meses). Los resultados en SG pueden haber sido influidos por dos factores: primero, el corto periodo de seguimiento con el consiguiente bajo número de eventos, apenas un 26% y 22% para el grupo de placebo y regorafenib, y segundo, el cruce de pacientes desde el brazo de placebo al grupo de tratamiento con regorafenib (84% de los pacientes pasaron al brazo de regorafenib en el momento del primer análisis de SLP). Este último factor, el cruce de pacientes, podría ser la causa de que en un análisis actualizado de los resultados de SG 2 años después del primer análisis y con un 73% y 68% de eventos para placebo y regorafenib respectivamente, no se observasen diferencias en SG, aunque el ajuste en función del cruzamiento por distintos métodos tampoco mostró diferencia estadísticamente significativa en la SG. Por todo ello, los resultados de SG son de difícil interpretación.
Hasta la fecha no existen tratamientos autorizados para los pacientes previamente tratados con imatinib y sunitinib. Los datos que recoge la bibliografía provienen en su inmensa mayoría de pequeños estudios fase II y estudios retrospectivos. Un estudio fase III (estudio ENEST) evaluó la eficacia de nilotinib vs. mejor terapia de soporte (BSC) tras fallo de imatinib y sunitinib (11). En este estudio fueron aleatorizados (2:1) 248 pacientes. La SLP fue la variable principal, la cual no mostró diferencias entre los brazos de tratamiento (nilotinib 109 días, BSC 111 días; P=0,56). Los resultados de SG tampoco mostraron diferencias (332 vs. 280 días; HR = 0,79, IC 95% (0,52–1,22)) si bien en un análisis exploratorio a posteriori en el subgrupo de pacientes tratados con nilotinib en una tercera línea real, reveló diferencias en SG (405 vs 280 días; HR = 0,67, IC 95% (0,48, 0,95)).
Respecto a la SG, y pese a las limitaciones que comportan las comparaciones indirectas, la supervivencia mediana que se observa en el estudio de regorafenib es superior a las medianas de SG descritas en otros estudios en tercera línea. En un estudio observacional en pacientes tratados con nilotinib, sorafenib e imatinib en 3ª línea (12), se observó una mediana de supervivencia de 9,3 meses (IC95%, 7,5–10,9).
El estudio RIGHT (13) evaluó el retratamiento con imatinib en pacientes previamente tratados con al menos imatinib y sunitinib. 41 pacientes fueron retratados con imatinib 400 mg frente a 40 pacientes tratados con placebo. La mediana de SGfue estimada en 8,2 meses para el grupo de imatinib y 7,5 para el grupo de placebo, sin diferencias significativas (HR 1,00; IC 95% 0,58–1,83). El 93% de los pacientes del grupo de placebo recibió tratamiento posterior con imatinib.
Tan sólo sorafenib ha mostrado tasas de supervivencia similares a las descritas para regorafenib (alrededor de los 18 meses) (14) y tasas de respuesta de alrededor del 10% si bien los datos provienen de estudios retrospectivos en cohortes de pacientes.
CONCLUSIÓN
No es posible establecer comparaciones con otros medicamentos utilizados en la práctica clínica para el tratamiento de los tumores del estroma gastrointestinal (GIST) irresecables o metastásicos tras progresión, si bien la calidad de los datos obtenidos para regorafenib es mayor que la de sus posibles comparadores.
Regorafenib podría considerarse tratamiento de elección en aquellos pacientes que progresen al tratamiento previo con imatinib y sunitinib o no los toleren y que presenten un estado general ECOG 0-1.
REFERENCIAS
1. Martí Obiol R, Garcés Albir M, López Mozos F, Ortega Serrano J. [Surgical treatment of gastrointestinal stromal tumours. Analysis of our experience]. Cir Esp. 2013 Jan;91(1):38-43
2. Fletcher CD, Berman JJ, Corless C, Gorstein F, Lasota J, Longley BJ, et al. Diagnosis of gastrointestinal stromal tumors: a consensus approach. Hum Pathol. 2002; 33:459-65
3. Rubió-Casadevall J, Borràs JL, Carmona C, Ameijide A, Osca G, Vilardell L, Izquierdo A, et al. Temporal trends of incidence and survival of sarcoma of digestive tract including Gastrointestinal Stromal Tumours (GIST) in two areas of the north-east of Spain in the period 1981-2005: a population-based study. Clin Transl Oncol. 2014 Jul;16(7):660-7
4. Gastrointestinal stromal tumours: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol (2014) 25 (suppl 3): iii21-iii26
5. Joensuu H. Adjuvant treatment of GIST: patient selection and treatment strategies. Nat Rev Clin Oncol. 2012;9(6):351-8
6. Poveda A, Rivera F, Martín J; Spanish Group for Sarcoma Research (GEIS); SEOM (Spanish Society of Clinical Oncology). SEOM guidelines for gastrointestinal stromal sarcomas (GIST). Clin Transl Oncol. 2012 Jul;14(7):536-40.
7. Le Cesne A, Blay JY, Reichardt P, Joensuu H. Optimizing tyrosine kinase inhibitor therapy in gastrointestinal stromal tumors: exploring the benefits of continuous kinase suppression. Oncologist. 2013;18(11):1192-9.
8. Ficha técnica de regorafenib. Disponible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002573/WC500149164.pdf (acceso en Noviembre 2014)
9. Informe publico de evaluación (EPAR) de la Agencia Europea del Medicamento (EMA). Diponible en: http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Assessment_Report_-_Variation/human/002573/WC500173131.pdf (acceso Noviembre 2014)
10. Demetri GD, Reichardt P, Kang YK, Blay JY, Rutkowski P, Gelderblom H, et al., Efficacy and safety of regorafenib for advanced gastrointestinal stromal tumours after failure of imatinib and sunitinib (GRID): an international, multicentre, randomised, placebo-controlled, phase 3 trial. Lancet. 2013 Jan 26;381(9863):295-302.
11. Reichardt P, Blay JY, Gelderblom H, Schlemmer M, Demetri GD, Bui-Nguyen B, et al. Phase III study of nilotinib versus best supportive care with or without a TKI in patients with gastrointestinal stromal tumors resistant to or intolerant of imatinib and sunitinib. Ann Oncol. 2012 Jul;23(7):1680-7.
12. Italiano A, Cioffi A, Coco P, Maki RG, Schöffski P, Rutkowski P, et al., Patterns of care, prognosis, and survival in patients with metastatic gastrointestinal stromal tumors (GIST) refractory to first- line imatinib and second-line sunitinib. Ann Surg Oncol. 2012 May;19(5):1551-9
13. Kang YK, Ryu MH, Yoo C, Ryoo BY, Kim HJ, Lee JJ, et al., Resumption of imatinib to control metastatic or unresectable gastrointestinal stromal tumours after failure of imatinib and sunitinib (RIGHT): a randomised, placebo-controlled, phase 3 trial. Lancet Oncol. 2013 Nov;14(12):1175-82
14. Montemurro M, Gelderblom H, Bitz U, Schütte J, Blay JY, Joensuu H, et al., Sorafenib as third- or fourth-line treatment of advanced gastrointestinal stromal tumour and pretreatment including both imatinib and sunitinib, and nilotinib: A retrospective analysis. Eur J Cancer. 2013 Mar;49(5):1027-31
GRUPO DE EXPERTOS
(por orden alfabético)
Agencia Española de Medicamentos y Productos Sanitarios
Comunidad Autónoma de Castilla-La Mancha
Comunidad Autónoma del Principado de Asturias
Todos los expertos han realizado una declaración de conflictos de interés.
El Laboratorio Titular, la Sociedad Española de Oncología Médica, Sociedad Española de Farmacología Clínica, Sociedad Española de Farmacia Hospitalaria y el Grupo Español de Pacientes con Cáncer, han tenido oportunidad de enviar comentarios al documento, si bien el texto final es el adoptado por el GCPT.
Fuente: Agencia Española de Medicamentos y Productos Sanitarios.
