Informe de Posicionamiento Terapéutico de ixekizumab (Taltz®) en el tratamiento de la psoriasis en placas
INFORME DE POSICIONAMIENTO TERAPÉUTICO
Informe de Posicionamiento Terapéutico de ixekizumab (Taltz®) en el tratamiento de la psoriasis en placas
IPT, 54/2016
Versión 1
Fecha de publicación: 21 de noviembre de 2016 †
La psoriasis es una enfermedad cutánea inflamatoria crónica y recurrente que afecta a un 1,5-3% de la población general en Europa (1). En los últimos años, se ha confirmado la asociación de las formas graves de psoriasis con una serie de comorbilidades que tienen un marcado impacto sobre el riesgo cardiovascular de los pacientes, lo que justifica que sea considerada como una enfermedad sistémica con manifestaciones predominantemente cutáneas. Asimismo, se reconoce actualmente la asociación de la psoriasis grave con un deterioro importante de la calidad de vida de los pacientes afectos, debido a su impacto en los ámbitos físico, emocional, sexual y económico.
El diagnóstico es clínico y en la mayoría de los casos no precisa confirmación histológica. La psoriasis en placas o vulgar es la forma más frecuente y representa en torno al 85-90% de los casos. Se caracteriza por la presencia de placas sobreelevadas eritemato- descamativas, bien delimitadas, generalmente distribuidas de forma simétrica en zonas de extensión de las extremidades, cuero cabelludo y, en menor medida, a nivel palmo-plantar. Hasta en un 30% de los casos se desarrolla artropatía inflamatoria (artritis psoriásica) (2,3).
En la mayoría de los casos (70%), la enfermedad sigue un curso crónico, con actividad inflamatoria persistente que suele exacerbarse en brotes.
La psoriasis en placas se puede clasificar en leve, moderada o grave, según la extensión y localización de las lesiones. En la mayoría de los pacientes la enfermedad se manifiesta de forma benigna, pero hasta en un 30% de los casos puede ser moderada ó grave y llegar a producir discapacidad física, psicológica o social (4). Algunos pacientes pueden presentar enfermedades concomitantes como la obesidad y enfermedades cardiovasculares (5,6).
Los objetivos del tratamiento de la psoriasis serían tanto el control mantenido de la afectación cutánea, como el control de la inflamación sistémica a largo plazo y la prevención de la aparición y progresión de comorbilidades sistémicas. Aunque no existe un tratamiento curativo, los tratamientos disponibles consiguen frenar su evolución, con un control adecuado de los síntomas y signos de forma duradera.
Habitualmente, la psoriasis leve a moderada o de extensión limitada se maneja con tratamiento tópico. Las formas moderadas a graves se definen por PASI >10 y/o afectación de superficie corporal (BSA)>10 y/o afectación importante de la calidad de vida (DLQI>10), y suelen requerir tratamiento sistémico. La presencia de artritis psoriásica o la afectación de zonas con compromiso funcional o estético como manos, pies y cara puede son también indicaciones potenciales de tratamiento sistémico (7,8).
Los tratamientos tópicos incluyen el uso de agentes emolientes, queratolíticos, retinoides tópicos, análogos de la vitamina D, corticoides e inmunomoduladores tópicos como tacrolimus/pimecrólimus. Entre los tratamientos sistémicos aprobados para su uso en la psoriasis moderada/grave se incluyen la fototerapia (radiación ultravioleta: ultravioleta A, ultravioleta B [UVB] o UVB de banda estrecha), fotoquimioterapia (psoralenos más radiación ultravioleta A), agentes inmunosupresores sistémicos (ciclosporina, metotrexato, acitretina y apremilast) y agentes biológicos (adalimumab, etanercept, infliximab, ustekinumab, y secukinumab).
IXEKIZUMAB XEKIZUMAB (TALTZ ® )
Ixekizumab es un anticuerpo monoclonal humanizado (IgG4) contra la IL-17A, citoquina proinflamatoria a la que se concede un papel principal en la patogenia de las enfermedades inflamatorias sistémicas como la psoriasis (9).
Ixekizumab está indicado en el tratamiento de la psoriasis en placas de moderada a grave en adultos candidatos a tratamiento sistémico. La dosis recomendada es de 160mg por vía subcutánea (dos inyecciones de 80mg) en la semana 0, seguido de 80 mg (una inyección) en las semanas 2, 4, 6, 8, 10 y 12, y posteriormente tratamiento de mantenimiento de 80mg (una inyección) cada 4 semanas. De acuerdo con su ficha técnica, el tratamiento debe discontinuarse en caso de ausencia de respuesta entre las semanas 16-20 de tratamiento.
Eficacia
La eficacia y seguridad de ixekizumab se ha evaluado en tres ensayos clínicos aleatorizados, doble ciego y controlados con placebo. Estos estudios incluyeron pacientes adultos con psoriasis en placas de moderada a grave candidatos a fototerapia o tratamiento sistémico (UNCOVER-1, UNCOVER-2, and UNCOVER-3). En los estudios UNCOVER 2 y 3 se incluyó una comparación frente a etanercept. En los estudios UNCOVER-1 y 2, los pacientes respondedores (sPGA 0,1) a la semana 12 de tratamiento con ixekizumab fueron aleatorizados a recibir placebo o ixekizumab durante 48 semanas adicionales; los pacientes aleatorizados a placebo, etanercept o ixekizumab no respondedores a semana 12 recibieron ixekizumab hasta 48 semanas adiciones (10, 11).
Se incluyeron un total de 3.866 pacientes en estos estudios, de los cuales el 64% habían recibido terapia sistémica previa (con agentes biológicos o inmunosupresores tradicionales, psoralenos y PUVA), 43,5% había recibido fototerapia previa, 49,3% terapia sistémica convencional y 26,4% había sido tratado con agentes biológicos. El 23,4% de los pacientes tenía historia de artritis psoriásica en el momento de su inclusión en los estudios. La mediana basal de puntuación en la escala PASI estaba entre 17,4 y 18,3; entre el 48,3% y el 51,2% de los pacientes tenían una puntuación entre grave y muy grave en el sPGA en la basal.
La variable primaria de eficacia fue la diferencia frente a placebo en la proporción de pacientes que alcanza una respuesta PASI 75 y PGA 0 (“blanqueamiento”) o 1 (“mínima”) a la semana 12.
Resultados de eficacia a la semana 12
(Figuras y tablas tomadas de la ficha técnica)
El estudio UNCOVER-1 incluyó un total de 1.296 pacientes, aleatorizados (1:1:1) a recibir placebo o ixekizumab durante 12 semanas (80mg cada 2 o 4 semanas tras una dosis inicial de 160mg) (Tabla 1).
† Fecha de adopción de la fase I del informe por el GCPT: 7 de junio de 2016
Tabla 1. Resultados de eficacia a la semana 12 en el estudio UNCOVER-1
| Variables | Número de pacientes (%) | ||
| Placebo (N = 431) | Taltz 80 mg Q4W(N = 432) | Taltz 80 mg Q2W (N = 433) | |
| sPGA de “0” (blanqueamiento completo)ó “1” (afectación mínima) | 14 (3,2) | 330 (76,4)a | 354 (81,8)a |
| sPGA de “0” (blanqueamiento completo) | 0 | 149 (34,5)a | 160 (37,0)a |
| PASI 75 | 17 (3,9) | 357 (82,6)a | 386 (89,1)a |
| PASI 90 | 2 (0,5) | 279 (64,6)a | 307 (70,9)a |
| PASI 100 | 0 | 145 (33,6)a | 153 (35,3)a |
| Reducción ≥ 4 en la itch NRSb | 58 (15,5) | 305 (80,5)a | 336 (85,9)a |
Abreviaturas: N = número de pacientes pertenecientes a la población por intención de tratar. Nota: los pacientes para los que faltaban datos se asignaron a la clasificación como no respondedores.
a p < 0,001 comparado con placebo.
b Pacientes con una puntuación en la itch NRS >= 4 en el basal: placebo N = 374, Taltz ® 80 mg Q4W N = 379, Taltz ® 80 mg Q2W N = 391.
El estudio UNCOVER-2 incluyó un total de 1.224 pacientes, aleatorizados (1:2:2:2) a recibir placebo o ixekizumab (80mg cada 2 o 4 semanas tras una dosis inicial de 160mg) o etanercept (50 mg dos veces por semana), durante 12 semanas (Tabla 2).
Tabla 2. Resultados de eficacia a la semana 12 en el estudio
UNCOVER-2
| Variables | Número de pacientes (%) | |||
| Variables | Placebo (N = 168) | Taltz 80 mg Q4W (N = 347) | Taltz 80 mg Q2W (N = 351) | Etanercept 50 mg dos veces a la semana (N = 358) |
| sPGA de “0” (blanqueamiento completo) ó “1” (afectación mínima) | 4 (2,4) | 253 (72,9) a | 292 (83,2) a | 129 (36,0) |
| sPGA de “0” (blanqueamiento completo) | 1 (0,6) | 112 (32,3) a,b | 147 (41,9) a,b | 21 (5,9)c |
| PASI 75 | 4 (2,4) | 269 (77,5) a | 315 (89,7) a | 149 (41,6) a |
| PASI 90 | 1 (0,6) | 207 (59,7) a,b | 248 (70,7) a,b | 67 (18,7) a |
| PASI 100 | 1 (0,6) | 107 (30,8) a,b | 142 (40,5) a,b | 19 (5,3) c |
| Reducción ≥ 4 en la itch NRS d | 19 (14,1) | 225 (76,8) a,b | 258 (85,1) a,b | 177 (57,8) a |
Abreviaturas: N = número de pacientes pertenecientes a la población por intención de tratar. Nota: los pacientes para los que faltaban datos se asignaron a la clasificación como no respondedores.
a p < 0,001 comparado con placebo.
b p < 0,001 comparado con etanercept.
c p < 0,01 comparado con placebo.
d Pacientes con una puntuación en la itch NRS >= 4 en el basal: placebo N = 135, Taltz ®
80 mg Q4W N = 293, Taltz ® 80 mg Q2W N = 303, Etanercept N = 306.
El estudio UNCOVER-3 incluyó un total de 1.346 pacientes, aleatorizados (1:2:2:2) a recibir placebo o ixekizumab (80mg cada 2 o 4 semanas tras una dosis inicial de 160mg) o etanercept (50 mg dos veces por semana) durante 12 semanas (Tabla 3).
Tabla 3. Resultados de eficacia a la semana 12 en el estudio
UNCOVER-3
| Variables | Número de pacientes (%) | |||
| Variables | Placebo Placebo (N = 193) | Taltz 80 mg Q4W(N = 386) | Taltz 80 mg Q2W (N = 385) | Etanercept 50 mg dos veces a la semana (N = 382) |
| sPGA de “0” (blanqueamiento completo) ó “1” (afectación mínima) | 13 (6,7) | 291 (75,4)a,b | 310 (80,5)a,b | 159 (41,6)a |
| sPGA de “0” (blanqueamiento completo) | 0 | 139 (36,0)a,b | 155 (40,3)a,b | 33 (8,6)a |
| PASI 75 | 14 (7,3) | 325 (84,2)a,b | 336 (87,3)a,b | 204 (53,4)a |
| PASI 90 | 6 (3,1) | 252 (65,3)a,b | 262 (68,1)a,b | 98 (25,7)a |
| PASI 100 | 0 | 135 (35,0)a,b | 145 (37,7)a,b | 28 (7,3)a |
| Reducción ≥ 4 en la itch NRS c | 33 (20,9) | 250 (79,9)a,b | 264 (82,5)a,b | 200 (64,1)a |
Abreviaturas: N = número de pacientes pertenecientes a la población por intención de tratar. Nota: los pacientes para los que faltaban datos se asignaron a la clasificación como no respondedores.
a p < 0,001 comparado con placebo.
b p < 0,001 comparado con etanercept.
c Pacientes con una puntuación en la itch NRS >= 4 en el basal: placebo N = 158, Taltz ® 80 mg Q4W N = 313, Taltz ® 80 mg Q2W N = 320, Etanercept N = 312.
Ixekizumab produjo una respuesta rápida, con una reducción del
50% en el PASI a la semana 2 de tratamiento y diferencias significativas en el PASI 75 frente a placebo y etanercept tras la
primera semana de tratamiento (Figura 1).
Figura 1. Puntuación PASI, porcentaje de mejoría de cada visita tras el basal (modified Baseline Observed Carried Forward, mBOCF por sus siglas en inglés) en la población por intención de tratar durante el periodo de inducción de dosis- UNCOVER-2 y UNCOVER-3
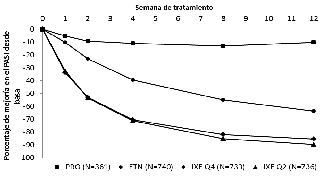
La superioridad de la eficacia de ixekizumab frente a placebo durante el periodo de inducción se demostró en todos los subgrupos de pacientes analizados. Estos incluyeron aspectos como características demográficas (edad, género, raza, peso y región geográfica), de la enfermedad (tratamientos previos recibidos, gravedad, edad de inicio y uso de terapia tópica concomitante), así como la localización de la enfermedad (uñas, cuero cabelludo). Por su relevancia, cabe mencionar que entre un 25-30% de los pacientes incluidos habían recibido tratamiento previo con fármacos biológicos; no se encontraron diferencias relevantes en las tasas de respuesta entre estos pacientes y aquellos que no habían recibido tratamiento con fármacos biológicos (sPGA 0,1) tras uso de biológicos fue 1,6% placebo, 67,8% ixekizumab Q4W y 79,7% ixekizumab Q2W vs 5%, 77,6% y 82,6% en placebo, ixekizumab Q4W y Q2W, respectivamente, en pacientes que no habían recibido tratamiento con fármacos biológicos; PASI 75 tras uso de fármacos biológicos fue 2,7%, 77,5% y 89,5% en placebo, ixekizumab Q4W e ixekizumab Q2W, respectivamente vs 5,2%, 83,1% y 88,4% en placebo, ixekizumab Q4W y Q2W, respectivamente, en pacientes que no habían recibido tratamiento con fármacos biológicos). Como cabe esperar se observó una tendencia a tasas de respuesta más bajas en los pacientes previamente tratados con múltiples fármacos biológicos (uso previo de ≥3 fármacos biológicos: PASI 75 4,3% placebo vs 73,3% y 86,2% en ixekizumab Q4W y Q2W, respectivamente, y sPGA 0% placebo vs 55,6% y 70,7% en ixekizumab Q4W y Q2W, respectivamente).
Los pacientes aleatorizados a ixekizumab durante el periodo inicial de 12 semanas que alcanzaron una respuesta PGA 0/1 en los estudios UNCOVER 1 y 2, fueron re-aleatorizados a recibir placebo o ixekizumab (80mg cada 4 o cada 12 semanas) durante un periodo adicional de 48 semanas. Los resultados de estos estudios muestran la eficacia de ixekizumab en el mantenimiento de la respuesta a largo plazo (68,7-78,3% pacientes con sPGA 0/1 a la semana 60, para la pauta de mantenimiento administrada cada 4 semanas), de forma consistente en todos los subgrupos de pacientes, incluidos los definidos en base al tratamiento previo recibido. En el grupo de pacientes aleatorizado a recibir placebo, la mediana de tiempo hasta la recaída (sPGA ≥3) fue de 164 días (datos agrupados para ambos estudios). De éstos, un 71,5% recuperó la respuesta sPGA (0,1) a las 12 semanas de reintroducir el tratamiento con ixekizumab 80 mg cada 4 semanas.
Se observó una mejoría significativa frente a placebo y etanercept a la semana 12 de tratamiento en lesiones ungüeales, en cuero cabelludo y a nivel palmoplantar. Esta mejoría se mantuvo hasta la semana 60 en aquellos pacientes que continuaron tratamiento con ixekizumab.
En cuanto a la valoración del paciente de la eficacia del tratamiento, ixekizumab produjo una mejoría estadísticamente significativa frente a placebo en la calidad de vida de los pacientes medido por el índice de calidad de vida en dermatología (DLQI) (ixekizumab 80 mg cada 2 semanas de -10,2 a -11,1, ixekizumab 80 mg cada 4 semanas de -9,4 a -10,7, etanercept de -7,7 a -8,0 y placebo -1,0 a -2,0). Además, ixekizumab se asoció con una mejoría estadísticamente significativa en la gravedad del picor medido por una escala numérica (reducción ≥ 4 puntos a la semana 12 en la escala numérica 84,6% ixekizumab cada 2 semanas, 79,2% ixekizumab cada 4 semanas y 16,5% placebo), que se mantuvo a largo plazo.
Seguridad
En general, el perfil de seguridad de ixekizumab está dentro de lo esperable por su mecanismo de acción y es muy similar al de etanercept, comparador activo en los estudios presentados.
La tasa de eventos adversos durante las 12 semanas iniciales de tratamiento fue muy similar a etanercept (44%, 57,5%, 57,8% y 54% en placebo, ixekizumab 80mg cada 4 semanas, ixekizumab 80mg cada dos semanas y etanercept, respectivamente).
Los efectos adversos más comunes en las 12 semanas iniciales de tratamiento con ixekizumab fueron nasofaringitis, infecciones del tracto respiratorio superior, reacciones en el sitio de inyección, y cefalea, todas ellas reportadas con tasas más altas que placebo. El perfil de seguridad fue similar durante la fase de mantenimiento, aunque la tasa de eventos fue menor.
Debido al mecanismo de acción de ixekizumab, tanto las infecciones como las reacciones de hipersensibilidad grave constituyen los riesgos identificados más relevantes. La incidencia de infecciones relacionadas con el tratamiento fueron del 22,9% en >placebo vs 27,0% y 27,4% para ixekizumab 80 cada 2 semanas y 80 mg (cada 4 semanas, respectivamente), incluyendo infecciones oportunistas, fundamentalmente candidiasis. El tratamiento está contraindicado en sujetos con infecciones agudas graves como la tuberculosis activa.
La incidencia de reacciones de hipersensibilidad durante el periodo de inducción, excluyendo las reacciones en el lugar de la inyección, fueron del 3,4% en ixekizumab vs 1,9% en placebo.
Se han descrito casos nuevos y reactivaciones de enfermedad inflamatoria intestinal, por lo que se recomienda precaución en estos pacientes y un seguimiento estrecho. Asimismo, el posible riesgo de desarrollo de neoplasias y eventos cardiovasculares mayores serán seguidos de forma particular durante el periodo post- comercialización.
Se ha acordado un plan de gestión de riesgos para ixekizumab que incluye un estudio observacional para el seguimiento de mujeres embarazadas en tratamiento con ixekizumab y un registro de pacientes con psoriasis que se espera generará información sobre los riesgos potenciales y sobre el uso del fármaco en poblaciones insuficientemente estudiadas como son ancianos, pacientes con infecciones activas, insuficiencia renal o hepática graves.
Aproximadamente entre un 9–17% de los pacientes tratados con ixekizumab (inducción y mantenimiento) desarrollaron anticuerpos frente al fármaco. De ellos, un 1% fueron neutralizantes asociados a concentraciones bajas del fármaco y baja respuesta clínica. Se ha acordado un seguimiento de la inmunogenicidad asociada a ixekizumab dentro del plan de gestión de riesgos.
Asimismo, existe un plan de desarrollo clínico en marcha acordado con las autoridades reguladoras para estudiar la eficacia y seguridad de ixekizumab en la población pediátrica.
DISCUSIÓN
El objetivo del tratamiento de la psoriasis en la práctica clínica es conseguir y mantener a largo plazo un blanqueamiento lo más amplio posible de las lesiones. Las guías clínicas actuales, teniendo en cuenta aspectos no sólo clínicos sino también de costes, recomiendan el uso de terapia sistémica con fármacos convencionales como primer escalón en la mayoría de los pacientes con indicación de tratamiento sistémico; el uso de fármacos biológicos se reserva para aquellos pacientes que no responden adecuadamente o presentan contraindicaciones o intolerancia a dichos tratamientos, incluido terapia PUVA.
Esta aproximación por pasos parece bien justificada en el caso particular de la psoriasis, dado que en la mayoría de los sujetos puede considerarse una enfermedad relativamente benigna y el retraso en implementar un tratamiento efectivo, generalmente, no conlleva consecuencias graves para el paciente.
Ixekizumab ha demostrado de forma robusta y convincente una elevada eficacia en el tratamiento de pacientes adultos con psoriasis en placas de moderada a grave previamente tratados con fototerapia, tratamiento tópico y/o terapia sistémica, incluidos fármacos biológicos. Los resultados se consideran clínicamente relevantes en todas las poblaciones estudiadas.
El perfil de seguridad de ixekizumab es favorable a corto y medio plazo, y por el momento no ha mostrado ningún problema de seguridad nuevo o inesperado respecto al perfil conocido de otros fármacos biológicos. Debe considerarse que, al tratarse del segundo fármaco de un nuevo grupo terapéutico de reciente introducción en el mercado, persisten las incertidumbres propias sobre su seguridad a largo plazo. Estas deberán estudiarse en el periodo post- comercialización mediante los resultados de los estudios en marcha y el registro de reacciones adversas notificadas.
Debido al nivel de eficacia demostrado por ixekizumab, incluso en pacientes con fallo a tratamientos sistémicos previos, incluidos fármacos biológicos, y teniendo en cuenta su perfil de seguridad, las autoridades reguladoras europeas han considerado el balance beneficio/riesgo favorable en pacientes con psoriasis en placas de moderada a grave en los que está indicado el tratamiento sistémico. Esta indicación coincide con la autorizada para secukinumab (12).
Actualmente no existen comparaciones directas con otras alternativas de tratamiento existentes en la actualidad más allá de las comparaciones con etanercept presentadas, lo que representa una limitación para poder caracterizar su eficacia/seguridad relativa frente a otras alternativas existentes.
La eficacia de las distintas opciones terapéuticas se ha comparado de forma directa o indirecta en diferentes revisiones sistemáticas (13,14). Los criterios empleados con mayor frecuencia para la comparación son los porcentajes de pacientes que alcanzan una respuesta PASI 75, PASI 90 y PASI 50 para cada uno de los fármacos disponibles, siendo el PASI 75 a las 12-24 semanas la variable principal en la inmensa mayoría de los estudios disponibles con fármacos biológicos. Los estudios que incluyen comparaciones directas apoyan la superioridad de infliximab y adalimumab sobre metrotexato, de ustekinumab y secukinumab sobre etanercept, (si bien en estos dos últimos estudios la superioridad se basa en una comparación a 12 semanas, insuficiente para observar la respuesta completa de etanercept) y de secukinumab sobre ustekinumab. Actualmente hay un estudio en marcha doble ciego comparativo con ustekinumab (15). En ausencia de comparaciones directas, se debe ser prudente a la hora de establecer conclusiones firmes sobre la posible superioridad de uno u otro fármaco en base a las tasas de respuesta a corto plazo; no pueden descartarse diferencias en las características basales de los sujetos de estudio e incluso del momento de evaluación de la respuesta, que expliquen al menos parcialmente algunas de las diferencias observadas. Incluso las comparaciones directas a corto plazo pueden desfavorecer a fármacos con un inicio de acción más lento, sin que esto implique necesariamente menor eficacia a largo plazo. El tratamiento de pacientes adultos con psoriasis de moderada a grave (candidatos a tratamiento sistémico de acuerdo con las guías de práctica clínica) debe realizarse de forma individualizada, teniendo en cuenta las características del paciente y el curso y momento evolutivo de la enfermedad (16). Atendiendo a las recomendaciones clínicas actuales, el puesto en terapéutica de ixekizumab, en línea con el primer fármaco de grupo secukinumab, y otros fármacos biológicos, sería tras el tratamiento con terapia sistémica convencional, restringido a pacientes que no respondan o bien presenten contraindicaciones o intolerancia a esos fármacos (ciclosporina, metotrexato o acitretina, o PUVA). En este contexto, ixekizumab se posiciona como una alternativa terapéutica con un mecanismo de acción diferente y una elevada eficacia en el blanqueamiento de las lesiones cutáneas, superior a algunos de los fármacos disponibles en segunda línea de tratamiento.
En casos excepcionales, debido a la gravedad y extensión de la enfermedad y al impacto que la misma tenga sobre el paciente concreto, podría considerarse un abordaje con ixekizumab como opción terapéutica tras un primer fracaso a tratamiento con fototerapia en pacientes candidatos a tratamiento sistémico.
CONCLUSIÓN ONCLUSIÓN
Ixekizumab se considera una opción terapéutica con una elevada eficacia a corto y medio plazo y un perfil de seguridad adecuadamente caracterizado. Además, su perfil de inmunogenicidad es relativamente bajo.
Es por tanto una alternativa terapéutica a otros biológicos en segunda línea de tratamiento de pacientes con psoriasis tras respuesta inadecuada, contraindicación o intolerancia a tratamientos convencionales o PUVA.
Además, en pacientes con una psoriasis extensa, grave e incapacitante, que requiere un abordaje con fármacos biológicos desde el inicio, ixekizumab podría ser una opción adecuada.
CONSIDERACIONES FINALES DEL GCPT
En la selección de ixekizumab u otros fármacos de elevada eficacia en esta indicación, será necesario considerar criterios de eficiencia.
ABREVIATURAS
PASI: Índice que mide superficie afectada y su gravedad. Se puntúa de 0-72. La respuesta PASI 50, 75, 90 significa el porcentaje de pacientes que alcanza una mejoría (reducción) en la puntuación basal del PASI ≥ 50, ≥75, ≥90. PASI 100 significaría un aclaramiento completo de las lesiones. No respuesta sería mejoría PASI <50.
sPGA: (static physician global assessment). Escala que se utilizar para medir la mejoría global durante el tratamiento de acuerdo con la impresión del médico sobre los cambios en la gravedad de la induración, descamación y eritema. Se puntúa de 0 a 5, donde 0 indica blanqueamiento completo y 5 indica enfermedad grave.
IGA mod 2011: Evaluación Global del Investigador (0-4).
BSA (body surface area): Superficie corporal afectada
DLQI (dermatology life quality index ): cuestionario estándar utilizado para evaluar la calidad de vida de pacientes con afectaciones dermatológicas.
mBOCF : de las siglas en ingles, modified Baseline Observation
Carried Forward.
REFERENCIAS
1. Christophers E. Psoriasis--epidemiology and clinical spectrum.
Clin Exp Dermatol. 2001 Jun;26(4):314-20.
2. Lebwhol M. Combining the new biologic agents with our current psoriasis armamentarium 2003. J Am Acad Dermatol 2003;49:S118-24.
3. Menter M. A, Griffiths C. Psoriasis: The Future. Dermatol Clin 2015;33: 161–166.
4. Koo J. Population-based epidemiologic study of psoriasis with emphasis on quality of life assessment. Dermatol Clin. 1996 Jul;14(3):485-96.
5. Mease P.J., Menter M.A. Quality-of-life issues in psoriasis and psoriatic arthritis: Outcome measures and therapies from a dermatological perspective. J Am Acad Dermatol 2006;54:685-704.
6. Sokoll KB, Helliwell PS. Comparison of disability and quality of life in rheumatoid and psoriatic arthritis. J Rheumatol. 2001 Aug;28(8):1842-6.
7. Menter M.A. et al. Guidelines of care for the management of psoriasis and psoriatic arthritis. J Am Acad Dermatol 2008;58:826-50.
8. Menter M.A. et al. Guidelines of care for the management of psoriasis and psoriatic arthritis. J Am Acad Dermatol 2011;65:137-74.
9. EPAR. Ficha técnica Taltz® (Ixekizumab). Disponible en:
www.aemps.es/cima.
10. Anti-interleukin-17 monoclonal antibody ixekizumab in chronic plaque psoriasis. Leonardi C, Matheson R, Zachariae C, et al. N Engl J Med. 2012; 366:1190-9.
11. Comparison of ixekizumab with etanercept or placebo in moderate-to-severe psoriasis (UNCOVER-2 and UNCOVER-3): results from two phase 3 randomised trials. Griffiths CE, Reich K, Lebwohl M, et al; UNCOVER-2 and UNCOVER-3 investigators. Lancet. 2015 ;386: 541-51.
12. Ficha técnica Cosentyx ® (secukinumab). Disponible en:
www.aemps.es/cima.
13. A Efficacy and safety of systemic treatments for moderate to severe posriasis: metanalysis of randomized controlled trials. Schmitt J, Rosumeck S, Thomaschewski G, Sporbeck B, Haufe E, Nast A. Br J Dermatol. 2014; 170 (2): 274.
14. Comparative efficacy of biological treatments for moderate to- severe psoriasis: a network meta-analysis adjusting for cross- trial differences in reference arm response. J.E. Signorovitch, K.A. Betts, Y.S. Yan, C. LeReun, M. Sundaram, E.Q. Wu and P. Mulani. Br J Dermatol 2015; 172, pp504–512.
15. A Study of Ixekizumab (LY2439821) in Participants With Moderate-to-Severe Plaque Psoriasis (IXORA-S). Clinicaltrials.gov.
16. Directrices españolas basadas en la evidencia para el tratamiento de la psoriasis con agentes biológicos, 2013. I . Consideraciones de eficacia y selección del tratamiento. L. Puiga, at al. Actas Dermosifiliogr. 2013;104:694-709. - Vol. 104 Núm.08 DOI: 10.1016/j.ad.2013.04.003.
GRUPO DE EXPERTOS
(por orden alfabético)
Agencia Española de Medicamentos y Productos Sanitarios
Centro de Información Farmacoterapéutica del Servizo Galego de Saúde
Comunidad Autónoma de Andalucía
Concepción Payares
Instituto de Investigación Sanitaria Puerta de Hierro. Farmacología Clínica.
Arantxa Sancho
Instituto de Investigación Sanitaria Puerta de Hierro. Farmacología Clínica. Representante de la AEMPS en el CHMP.
Todos los expertos han realizado una declaración de conflictos de interés.
El Laboratorio Titular, la Sociedad Española de Farmacia Hospitalaria, la Sociedad Española de Farmacología Clínica, La Sociedad Española de Reumatología, la Academia Española de Dermatología y Venerología y la Asociación de Pacientes de Psoriasis y Familiares han tenido oportunidad de enviar comentarios al documento, si bien el texto final es el adoptado por el GCPT.

